微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)按下图所示装置连接好仪器在U形管中加入饱和氯化铜溶液,用石墨棒作电极,接通电源,电解数分钟后,观察现象。
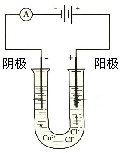
(1)接电源负极的石墨棒上现象??电极反应为??&s.5*u.c.#om?
(2)接电源正极的石墨棒上现象,??电极反应为??
电解反应的化学方程式?
(3)在上述电解反应中,被氧化的物质是?离子
(4)如何验证阳极产生的气体:?
参考答案:
(1)有红色金属Cu析出;Cu2+ +? 2e- =Cu
(2)放出黄绿色气体;2Cl- - 2e- =Cl2↑;CuCl2 ? Cu + Cl2↑
? Cu + Cl2↑
(3)Cl-
(4)把湿润的淀粉KI试纸放在阳极附近,试纸变蓝色
本题解析:略
本题难度:简单
2、选择题 铅蓄电池是典型的可充电电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:
 ?
?
有关该电池的说法正确的是?(?)
A.放电时,蓄电池内电路中H+ 向负极移动
B.放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4
C.充电时,阳极反应:PbSO4 +2e- = Pb + SO42-
D.充电时,铅蓄电池的负极与外接电源的负极相连
参考答案:
D
本题解析:略
本题难度:一般
3、选择题 有两只串联的电解池(Pt为电极),甲池盛有足量的CuSO4溶液,乙池盛有足量的某硝酸盐的稀溶液.电解时当甲池电极析出6.4gCu时,乙池电极析出21.6g金属,则乙池的溶质可能是( )
A.NaNO3
B.Cu(NO3)2
C.Al(NO3)3
D.AgNO3
参考答案:甲池盛有足量的CuSO4溶液,电解过程中,阴极上的电极反应为:Cu2++2e-=Cu,
当该电极析出6.4gCu即0.1molCu时,转移电子为0.2mol,在转移这些电子的情况下,乙池电极会析出21.6g金属,,设乙池析出金属M,其相对原子量为M,乙池中阴极反应为
? ?Mx++xe-=M,
?1?x? 1
? 0.2mol?2.16M?
则M和x的关系满足:1.08xM=0.1,
将四个选项的金属元素化合价x和相对原子量M代入上式,只有D符合,即x=1,M=108.
故选D.
本题解析:
本题难度:简单
4、填空题 Ⅰ.工业上常用电解饱和食盐水的方法制备氯气,其装置如图1所示,如果在饱和食盐水中滴加酚酞,通电后______?(填X或Y)极附近溶液变红,写出电解饱和食盐水的化学方程式______.再用氯气制备漂白粉,请写出漂白粉长期露置在空气中失效的反应的化学方程式______.
Ⅱ.请利用图2装置及试剂组装一套装置,其流程是先制取纯净干燥的Cl2(不收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性.
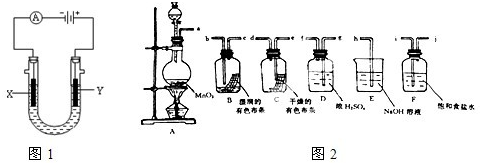
(1)按气体从左向右流向将各装置依次连接起来(填接口标号):a?接______,______接______,______接______,______接______,______接______.
(2)圆底烧瓶中发生反应的化学方程式是______.如果将过量二氧化锰与20mL?12mol?L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol.其主要原因为______.
(3)E装置的作用是______,F装置的作用是______.
(4)装置______(填“B”或“C”)中的有色布条褪色,以上事实说明起漂白作用的物质是______.
参考答案:Ⅰ.电解饱和食盐水的方法制备氯气,装置图中与电源正极连接的Y电极为阳极,溶液中氯离子失电子发生氧化反应生成氯气,与电源负极连接的X电极为电解池的阴极,溶液中氢离子得到电子发生还原反应,生成氢气,反应的化学方程式为2NaCl+2H2O?通电?.?2NaOH+H2↑+Cl2↑;阴极附近水的电离平衡因为氢离子减小,氢氧根离子浓度增大,溶液变红;氯气和消石灰反应生成氯化钙、次氯酸钙和水;漂白粉变质的原因是次氯酸钙和二氧化碳、水反应生成碳酸钙沉淀和次氯酸,反应的化学方程式为Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,故答案为:X;2NaCl+2H2O?通电?.?2NaOH+H2↑+Cl2↑;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
Ⅱ.(1)验装置的连接顺序为:发生装置→除杂装置→性质检验装置→尾气处理装置;因为收集的是气体,所以除杂装置中长导管进气,段导管出气;因为饱和食盐水中有水,浓硫酸有吸水性,所以先连接饱和食盐水装置后连接浓硫酸装置;试验干燥的Cl2和潮湿的Cl2有无漂白性,因为湿润的有色布条有水分,所以D装置先连接C后连接B,
故答案为:a→i→j→g→f→e→d→b→c→h;
(2)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水.随反应进行,浓盐酸浓度减小变稀后不能和二氧化锰反应生成氯气,
故答案为:MnO2+4HCl(浓)?△?.?MnCl2+Cl2↑+2H2O;反应一段时间后,盐酸浓度变稀,不能和二氧化锰就反应;
(3)浓盐酸有挥发性,浓盐酸中的水在加热的条件下变成水蒸气,所以氯气中混有氯化氢和水蒸气;氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可用氢氧化钠溶液吸收多余的氯气.氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水除去HCl气体,
故答案为:吸收多余的氯气防止污染空气;除去氯气中的HCl气体;
(4)氯气能水反应,反应方程式为:Cl2+H2O=H++Cl-+HClO,C瓶中的成分是氯气,不能使有色布条褪色,BB瓶中有次氯酸生成,使有色布条褪色,以上事实说明起漂白作用的物质是次氯酸,故答案为:B,次氯酸(HClO).
本题解析:
本题难度:一般
5、选择题 下图中A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,C为盛有稀硫酸的电解槽,e、f为Pt电极。接通电源后,发现d点显红色。下列有关说法正确的是
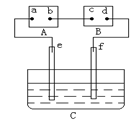
A.电源A上的a极是正极
B.d极上的电极反应方程式为2Cl--2e-=Cl2↑
C.e、f极上产生的气体体积比为2:1
D.C中溶液的pH增大
参考答案:C
本题解析:本题实质是两个电解池。接通电源后,发现d点显红色,说明呈碱性,即电解池的阴极:2H++2e-=H2↑;从而可知电池a极为负极,b极为正极;c、f为阳极,d、e为阴极;
电解食盐水:阴极::2H++2e-=H2↑?阳极:2Cl+-2e-=Cl2↑
电解硫酸:?阴极:2H++2e-=H2↑?阳极:4OH--4e-=2H2O+O2↑,随着水的逐渐减少,溶液酸性增强,pH减小。
本题难度:一般