| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《离子方程式的书写及正误判断》考点预测(2017年强化版)(四)
参考答案:A 本题解析:略 本题难度:一般 2、填空题 (6分) 酸性KMnO4、H2O2、NaClO在生产、生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸 (H2C2O4 )去除Fe(NO3)3也是重要氧化试剂,下面是对这三种氧化剂性质的探究。 参考答案: 本题解析:(1)过氧化氢与Cu在酸性条件下发生氧化还原反应,生成氯化铜和水,其中过氧化氢作氧化剂,得到2个电子,Cu作还原剂,失去2个电子,用双线桥表示为 本题难度:一般 3、选择题 下列反应的离子方程式书写不正确的是 |
参考答案:
本题解析:
本题难度:一般
4、填空题 写出下列反应的离子方程式,或相应的化学方程式(每题2分7小题共14分)
(1)石灰石溶于稀盐酸 。
(2)稀硫酸与氢氧化钡溶液的反应 。
(3)碳酸氢钠溶液与盐酸反应 。
(4)氢氧化铜与稀硫酸反应 。
(5)2H++ CO32-=CO2↑+H2O 。
(6)Cu+2Ag+=Cu2++2Ag 。
(7)CO2+2OH-=CO32-+H2O 。
参考答案:(1)CaCO3+2H+=Ca2++H2O+CO2↑
(2)2H++SO42-+2OH-+Ba2+=2H2O+BaSO4↓ (3)HCO3-+H+=H2O+CO2↑
(4)Cu(OH)2+2H+=Cu2++2H2O (5)Na2CO3+2HCl=2NaCl+H2O+CO2↑
(6)Cu+2AgNO3=Cu(NO3)2+2Ag (7)CO2+2NaOH=Na2CO3+H2O
本题解析:用实际参加反应的离子符号来表示反应的式子叫做离子反应方程式,判断离子方程式正确与否的方法一般是:(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式,据此可以写出有关的离子方程式或化学方程式。
(1)石灰石难溶于水,应该用离子符号来表示,则石灰石溶于稀盐酸的离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑
(2)稀硫酸与氢氧化钡溶液生成硫酸钡白色沉淀和水,因此二者反应的离子方程式为2H++SO42-+2OH-+Ba2+=2H2O+BaSO4↓。
(3)碳酸氢钠溶液与盐酸反应生成氯化钠、水和CO2,因此反应的离子方程式为HCO3-+H+=H2O+CO2↑。
(4)氢氧化铜难溶于水,应该用离子符号表示,则氢氧化铜与稀硫酸反应的离子方程式为Cu(OH)2+2H+=Cu2++2H2O。
(5)该反应2H++ CO32-=CO2↑+H2O表示可溶性碳酸盐与强酸反应准备CO2的离子方程式,则相应的化学反应可表示为Na2CO3+2HCl=2NaCl+H2O+CO2↑。
(6)该反应Cu+2Ag+=Cu2++2Ag表示金属铜与可溶性硝酸银发生的置换反应,则相应的化学方程式可表示为Cu+2AgNO3=Cu(NO3)2+2Ag。
(7)该反应CO2+2OH-=CO32-+H2O表示CO2与强碱反应生成可溶性碳酸盐和水的离子反应,则相应的化学方程式可表示为CO2+2NaOH=Na2CO3+H2O。
考点:考查离子方程式和化学方程式的书写
本题难度:一般
5、填空题 25℃时,将0.01 mol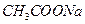 和0.002 mol
和0.002 mol 溶于水,形成1L混合溶液:
溶于水,形成1L混合溶液:
(1)该溶液中存在着三个平衡体系,用电离方程式或离子方程式表示:
① ;
② ;
③ 。
(2)溶液中共有七种不同的粒子(指分子和离子)。在这些粒子中,浓度为0.01 mol/L的是 ,浓度为0.002 mol/L的是 ; 和 两种粒子物质的量之和等于0.01 mol。
参考答案:(1)(每空2分) ① H2O H+ + OH-;
H+ + OH-;
② CH3COOH CH3COO- + H+;
CH3COO- + H+;
③ CH3COO- + H2O CH3COOH + OH-
CH3COOH + OH-
(2)(每空1分) Na+ , Cl-; CH3COO-和CH3COOH。
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《有机物燃烧.. | |