微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
试回答下列问题
⑴上述正向反应是???反应(填“放热”或“吸热”)。
⑵在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有???(选填A、B、C、D、E)。
?
| n(CO)
| n(H2O)
| n(H2)
| n(CO2)
|
A
| 1
| 5
| 2
| 3
|
B
| 2
| 2
| 1
| 1
|
C
| 3
| 3
| 0
| 0
|
D
| 0.5
| 2
| 1
| 1
|
E
| 3
| 1
| 2
| 1
|
⑶已知在一定温度下:
C(s)+CO2(g) 2CO(g)平衡常数K;
2CO(g)平衡常数K;
C(s)+H2O(g) CO(g)+H2(g)?平衡常数K1;
CO(g)+H2(g)?平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g)平衡常数K2;
H2(g)+CO2(g)平衡常数K2;
则K、K1、K2之间的关系是K=???。
⑷若在500℃时进行,设起始时CO和H2O的起始浓度均为0.010mol/L,在该条件下,CO的平衡转化率为:???。
⑸若反应在800℃进行,设起始时CO(g)和H2O(g)共为1mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=???。
参考答案:⑴放热?⑵BCD?⑶K1/K2?⑷75%?⑸X
本题解析:(1)根据表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,所以正方应是放热反应。
(2)由于反应前后体积不变,所以设容器的容积是1L,则ABCD中 的比值分别是
的比值分别是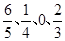 ,所以其中向正反应方向移动的有BCD。
,所以其中向正反应方向移动的有BCD。
(3)根据盖斯定律可知,①-②即得到C(s)+CO2(g) 2CO(g),所以该反应的平衡常数K=
2CO(g),所以该反应的平衡常数K=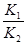 。
。
(4)? CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
起始浓度(mol/L) 0.010? 0.010? 0? 0
转化浓度(mol/L)? x? x? x? x
平衡浓度(mol/L)0.010-x? 0.010-x? x? x
则根据平衡常数表达式可知
解得x=0.0075mol/L
则在该条件下,CO的平衡转化率为75%
(5)? CO(g)+H2O(g) H2(g)+ CO2(g)
H2(g)+ CO2(g)
起始浓度(mol/L) 1-x? x? 0? 0
转化浓度(mol/L)(1-x)y?(1-x)y?(1-x)y (1-x)y
平衡浓度(mol/L)1-x-y+xy? x -y+xy?(1-x)y (1-x)y
则根据平衡常数表达式可知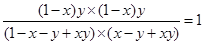
解得x=y
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
2、选择题 下列过程不用熵判据判断的是(?)
A.氯化铵与氢氧化钡晶体混合研磨,很快会闻到刺激性气味
B.冬天一杯热水很快变冷
C.有序排列的火柴散落时成为无序排列
D.多次洗牌以后,扑克牌毫无规律的混乱排列的几率大
参考答案:B
本题解析:B. 冬天一杯热水很快变冷,这是温度下降,热量散失的缘故,跟熵无关。
本题难度:一般
3、填空题 (14分)煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。
(1)已知:

①C(s) + H2O(g) === CO(g)+H2(g) ΔH=+131.3 kJ・mol-1
②CO2(g) + H2(g) ===" CO(g)" + H2O(g) ΔH=+41.3 kJ・mol-1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为 。
该反应在 (填“高温”、“低温”或“任何温度”)下有利于正向自发进行。
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g)  N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g)。向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
时间(min)
浓度(mol・L-1)
| 0
| 10
| 20
| 30
| 40
| 50
|
NO
| 1.00
| 0.68
| 0.50
| 0.50
| 0.60
| 0.60
|
N2
| 0
| 0.16
| 0.25
| 0.25
| 0.30
| 0.30
|
CO2
| 0
| 0.16
| 0.25
| 0.25
| 0.30
| 0.30
|
①10~20min内,N2的平均反应速率v(N2)= 。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母序号)。
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020 mol・L-1,在该条件下达到平衡时,CO的转化率为 。
(4)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
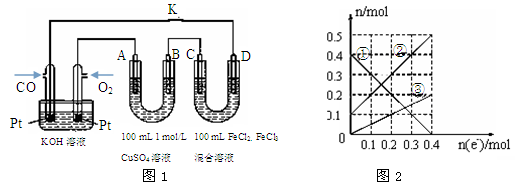
①乙中A极产生的气体在标准状况下的体积为________________。
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是________(填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要________ mL 5.0 mol・L-1 NaOH溶液。
参考答案:(1)C(s) + 2H2O(g) = CO2(g) + 2H2(g)
本题解析:
本题难度:困难
4、选择题 在一定条件下,向2L密闭容器中充入3molX气体和1molY气体发生下列反应:2X(g)+Y(g)?3Z(g)+2W(g),在某一时刻达到化学平衡时,测出的下列各生成物浓度的数据肯定错误的是( )
A.c(Z)=0.75mol?L-1
B.c(Z)=1.20mol?L-1
C.c(W)=0.80mol?L-1
D.c(W)=1.00mol?L-1
参考答案:可逆反应中,反应物不可能在反应中完全转化,由于反应中X、Y按照物质的量2:1反应,所以X过量1mol,生成3molZ,2molW,但反应不可能完全进行到底,所以0.5mol/L<C(X)<1.5mol/L;0<C(Z)<1.5mol/L;0<C(W)<1mol/L.
故选D.
本题解析:
本题难度:简单
5、计算题 将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下发生反应:
2SO2?+ O2 2SO3?达到平衡时,测得平衡混合物总的物质的量为5mol。
2SO3?达到平衡时,测得平衡混合物总的物质的量为5mol。
求:(1)平衡时O2的物质的量浓度;
(2)平衡时SO2的转化率;
(3)平衡时SO3的体积分数。
参考答案: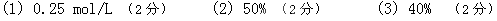
本题解析:? 2SO2?+ O2 2SO3?
2SO3?
起始量(mol)? 4? 2? 0
转化量(mol)? 2x? x? 2x
平衡量(mol)4-2x? 2-x? 2x
则根据题意可知4-2x+2-x+2x=5mol
解得x=1mol
所以平衡时O2的物质的量浓度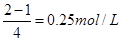
平衡时SO2的转化率为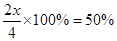
平衡时SO3的体积分数为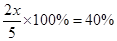
点评:该题是基础性试题的考查,难度不大,本题有助于培养学生的逻辑推理能力。该题的关键是让学生明确在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。
本题难度:一般