|
�߿���ѧ֪ʶ���ܽᡶ��ѧ��Ӧ����������Ƶ����̣�2017�����°棩(��)
2017-07-27 09:30:35
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���к��Ȳⶨ��ʵ���в���Ҫ�õ���������
A����Ͳ
B���¶ȼ�
C������������
D��������ƽ
|
�ο��𰸣�D
����������к��Ȳⶨ��ʵ��װ����ͼ
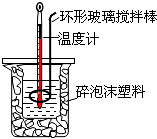
��Ҫ�¶ȼƲⶨ�¶ȡ����β������������ʹ��Һ��Ͼ��ȣ�����Ҫ��Ͳ��ȡһ�������ᡢ����Һ������Ҫ��ƽ��
���㣺�����к��Ȳⶨ��ʵ��װ�á�
�����Ѷȣ���
2������� �Իش������к��Ȳⶨ���й����⡣
��1��ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢���β����������0.50mol��L��1���ᡢ0.55mol��L��1 NaOH��Һ����ȱ�ٵ�ʵ����Ʒ��__________��
��2��ʵ�����ܷ��û���ͭ˿��������滷�β��������__________����ԭ����______________________________________________��
��3��ʵ��ʱ�������ἰNaOH��Һ�������Ϊ50mL������Һ�ܶ�Ϊ1g/cm3��������Һ�ı�����c��4.18J/(g����)��ʵ����ʼ�¶�Ϊt1�棬��ֹ�¶�Ϊt2�档���ƶ��к��ȵļ���ʽ����H��___________________________________��
�ο��𰸣���
��1���¶ȼ�
��2�����ܣ���Ϊͭ���кܺõĵ������ܣ���ʹ����ɢ����ȥ��ʹ�ⶨ���ƫС��
��3����H����1. 672��t2��t1��kJ/mol
������������⿼���к��ȵIJⶨ���йؼ��㣬�ر�ע�⣬�к��ȵIJⶨ��������ѡ��ʵ��ʱ��ע������к��ȵļ��㷽������������
�к��ȵIJⶨ����ؼ��ľ��DZ��¸��ȣ�Ҫ�����ܵķ�ֹ��������ʧ��������¶ȵIJ�����Ҫ�����ʼʱ����ߵ�ʱ���¶ȣ����ܵõ���Ӧǰ����¶ȱ仯ֵ���¶ȼƵľ�ȷ��Ҫ�����ܵĸߣ�ͬʱ�������ٶȻ�Ҫ�죬�������ܼ���ʵ����
ʵ���õ�������к�����һ�����ʵ���ˮʱ���ų��������������뻻�������1molˮʱ���ų������������к��ȡ���˼���ʱ�������¹�ʽ��ɡ�
��H����Q/n����cm��t/n? c��4.18J/(g����)��m��m1��m2��100g����t��(t2��t1)��nΪ�кͷ�Ӧ�����ɵ�ˮ�����ʵ�������λΪkJ/mol
�����Ѷȣ���
3��ѡ���� ���з�Ӧ����Ԫ��ȫ������ԭ����
A.MnO2+4HCl��Ũ��MnCl2+2H2O+Cl2��
B.Cl2+2NaOH=NaCl+NaClO+H2O
C.5Cl2+I2+6H2O=10HCl+2HIO3
D.Cu��OH��2+2HCl�TCuCl2+2?H2O
�ο��𰸣�C
�����������������Ӧ����Ԫ��ȫ������ԭ��ClԪ�صĻ��ϼ�Ӧ���ͣ�����ClԪ�ص������ڷ�Ӧ�б���Ϊ�����ԣ��Դ˽����⣮
���A����Ӧ��Cl���ϼ����ߣ������������ֱ���Ϊ���ԣ���A����
B����Ӧ��ClԪ�ػ��ϼۼ������ֽ��ͣ��ȱ������ֱ���ԭ����B����
C����Ӧ��ClԪ�ػ��ϼ۽��ͣ�����ԭ����C��ȷ��
D��ClԪ�ػ��ϼ�û�з����仯������������ԭ��Ӧ����D����
��ѡC��
���������⿼��������ԭ��Ӧ��Ϊ�߿���Ƶ���㣬ע���Ԫ�ػ��ϼ۱仯�ĽǶ���ʶ���ʱ��ֳ������ʣ���Ŀ�ѶȲ���
�����Ѷȣ�����
4��ѡ���� �ұ�ΪԪ�����ڱ��������е�һ���֣��й�Ԫ��X��Y��Z��M��˵������ȷ���ǣ�?��
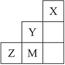

A��Y��Z���γ�ZY6����
B��X��������ԭ�Ӿ���
C��ԭ�Ӱ뾶��Z��M��Y
D��Z2-���ӵĽṹʾ��ͼ�ɱ�ʾΪ��
�ο��𰸣�B
�����������������Ԫ�ؾ�Ϊ������Ԫ�أ��ɵ�1����������Ԫ�ص�λ���ص��֪XΪHeԪ�أ���YΪFԪ�أ�MΪClԪ�أ�ZΪSԪ�ء�S���������Ϊ+6�����Կ���F�γ�SF6���ӣ�A����ȷ��ͬ���ڴ�����ԭ�Ӱ뾶��С��ͬ������ϵ���ԭ�Ӱ뾶������������C����ȷ��D����S���������Ӻ��γɼ�������S2-������D����ȷ����B����He����ϡ������Ԫ�أ��γɵľ����Ƿ��Ӿ��塣
�����Ѷȣ���
5��ѡ���� ��Ȩ�����ﱨ����1996���ѧ���������з���H3���ӣ��ס��ҡ���������λѧ���Դ˱�������ʶ��ȷ���ǣ�������
A������Ϊ�������־��Բ����ܣ���ΪH3����Υ���˹��ۼ�����
B������Ϊ�����л����ܴ�����һ���ⵥ�ʣ���Ϊ��Ԫ��������ͬλ�ر�Ȼ������ͬ��������
C������ΪH3����ʵ������H2������H+������ۼ���ϵIJ��Ӧд��H3+
D������Ϊ��������ķ��ִ��ڣ���֤����ͳ�ļۼ�������һ���ľ������д�������չ
�ο��𰸣�A�������۾���һ����ʱ���Ժ;����ԣ������з���H3���ӣ�����ڸ÷��ӣ���A����
B��ͬλ�ص�������ͬ��������������أ�����ܻ����ⵥ�ʣ�Ҳ����û�У���B����
C�������������Dz�ͬ����������H3���Ӳ���д��H3+����C����
D��H3���ӵĴ��ڣ����ô�ͳ�ļۼ����۲��ܽ��ͣ�����ͳ�ļۼ�������һ���ľ������д�������չ����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
|