��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��17�֣���A��B��C��D��E��Q����Ԫ�أ����ǵĺ˵������������A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��һ��Ԫ�أ�B��C��D��E����A��һ�����Ӳ㣬��B��C��D��E���������ڵ�����Ԫ�أ�����E��Ԫ�����ڱ��зǽ�������ǿ��һ��Ԫ�أ�Q�ĺ˵������A��B��D��E�ĺ˵�������ܺͣ���Ҫ������������⣺
�ţ��⼸��Ԫ���е縺�������ǣ�?������Ԫ�ط��ţ���ͬ����
�ƣ�B��C��D��E�ĵ�һ��������С�����˳���ǣ�?����ԭ�Ӱ뾶�ɴ�С��˳���ǣ�?����
�ǣ�C���⻯��ĵ���ʽ�ǣ�?����C���⻯��ṹʽ�ǣ�?����C������������Ӧ��ˮ����Ļ�ѧʽ�ǣ�?����C������������Ӧ��ˮ�����C����ͼ������γɵĻ�����Ļ�ѧʽ�ǣ�?����
�ȣ�Q�ĵ����Ų�ʽ�ǣ�?����Q�ļ۵����Ų�ʽ�ǣ�?����Q�ļ۵����Ų�ͼ�ǣ�?����
�ɣ�˵��D��Q�����ڱ��еķ�����D�ڣ�?������Q�ڣ�?����, Dԭ�Ӻ����У�?�����ɵ�����.
�ʣ�Ԫ��B�����ڱ���λ�ڵڣ�?�����ڣ��ڣ�?���塣
�ο��𰸣���17�֣���? F?
��C��O��N��F? C��N��O��F?��
��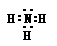 ? HNO3?
? HNO3?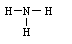 ?NH4NO3?��
?NH4NO3?��
��1S22S22P63S23P63d54S1��Ar��3d54S1? 3d54S1?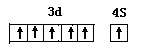 ?
?
��P? d? 2
�ʶ���2? IVA
�����������
�����Ѷȣ�һ��
2��ѡ���� �����£���pH=1��������Һƽ���ֳ����ȷݣ�һ�ݼ�������ˮ����һ�ݼ������������Һ���ʵ���Ũ����ͬ������������Һ������pH��������1��������ˮ������������Һ�������Ϊ(����)
A��5��1
B��6�� 1
C��10��1
D��11��1
�ο��𰸣�B
�����������ÿ��������Һ�����ΪV��ÿ����Һ��c(H+)=0.1mol/L��
һ�ݼ�ˮpH����1���ɵã�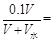 0.01��
0.01��
��һ�ݼ����������Ũ������������ҺpH����1���ɵã�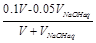 =0.01��
=0.01��
�����϶�ʽ���ˮ������������Һ�����Ϊ6��1��
������pH=��lgc(H+)��
�����Ѷȣ���
3��ѡ���� ����˵������ȷ���ǣ�?��
A������̼ԭ�������������ӣ�������̼��������������������������6/7
B�������ͬ���칹����2�֣���ϰ�������ֱ�Ϊ�������顢������
C��F 2��Cl2��Br2��I2�۵�����Է����������������
D��ԭ������Ϊ34�ŵ�Ԫ�����ڳ����ڵ�����Ԫ��
�ο��𰸣�B
����������������ͬ���칹����3�У��ֱ��������顢�����顢�����飬����ѡ��B����ȷ��
�����Ѷȣ���
4��ѡ���� N��������Ϊ14������NH3�У�����������������������֮��Ϊ
A��10:7: 11
B��10:11:9
C��10:11:8
D��10:10:7
�ο��𰸣�D
���������N��ԭ��������7������������7����������Ϊ17��7��7����Ϊ���������ں������������������NH3�У������������������������ֱ�Ϊ10��10��7������֮��Ϊ10:10:7������D��
�����Ѷȣ���
5��ѡ���� ������RO3n -�й���x ��������ӣ�R ԭ�ӵ�������ΪA ����R ԭ�Ӻ��ں��е�������Ϊ��?��
A�� A + n + 48 �C x
B��A + n + 24 �C x
C��A - n + 24 �C x
D��A - n - 24 �C x
�ο��𰸣�B
�����������RԪ�ص�������ΪZ����x=Z+8*3+n,��Z=X��24��n������R��������N=A��Z=A��X+24+n������B��ȷ��
�����Ѷȣ�һ��