| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ���⡶���ʵ���������Ԥ�⣨2017��ǿ���棩(��)
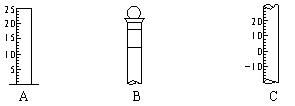 ����д���������������ƣ� A �� ��B �� ��C �� �� ������B�ϱ���� �� ������ţ��� ������ ���¶� �ۿ̶��� ��Ũ�� ���ݻ� �Ǽ�������B�Ƿ�©ˮ�ķ����� �� �ο��𰸣�(10��)�������� �� �ƻ�ѧ�� BC��ÿ��1�֣� ����������� �����Ѷȣ��� 2��ѡ���� ��NAΪ�����ӵ�������ֵ������������ȷ���� |
�ο��𰸣�D
���������A����״���£�0.1mol������ˮ��Ӧ�ǿ��淴Ӧ������δȫ��ת��Ϊ���������ת�Ƶĵ�����С��0.1NA������B�����³�ѹ��44g��������ʵ�����1mol��3��Cԭ��ֻ����2��C-C�������Ժ��е�̼̼������Ϊ2 NA������C����״����2molһ��������1mol������Ӧ����2mol������������������ķ����������2 NA������D������������������к��е��������������Ӹ����ȶ���2:1������1 mol Na2O��Na2O2������к��е�����������������3 NA����ȷ����ѡD��
���㣺���鰢��٤�������������Ĺ�ϵ
�����Ѷȣ�һ��
3��ѡ���� ʹ��ͬ���ʵ���Ũ�ȵ�NaCl��MgCl2��AlCl3��Һ�е�Cl��������ȫ����ʱ,��������ͬŨ�ȵ�AgNO3��Һ�������Ϊ3:2:1,������������Һ��������ǣ�?��
A��9:3:1
B��3:2:1
C��6:3:2
D��9:4:1
�ο��𰸣�A
�����������AgNO3��Һ��Ũ�ȶ���c������ֱ�Ϊ3V��2V��V��NaCl��MgCl2��AlCl3��Һ��Ũ�ȶ���c1��������ֱ�Ϊx��y��z����ȫ����ʱ������ӦCl��+Ag���TAgCl�����ɷ���ʽ��֪��
c1��x=c��3V��c1��2��y=c��2V��c1��3��z=c��V��
���x��y��z=9��3��1��ѡA��
�����Ѷȣ�һ��
4��ѡ���� NA��ʾ�����ӵ�����ֵ������˵����ȷ����
A��1mol Cu������ϡ���ᷴӦ����NA��NO����
B����״���£�2.24 L CHCl3�ķ�����Ϊ0.1 NA
C��t��ʱ��1L pH=6�Ĵ�ˮ�У���1��10-6NA��OH-
D����FeI2��Һ��ͨ����������������1mol Fe2+������ʱ���ܹ�ת�Ƶ��ӵ���ĿΪ1 NA
�ο��𰸣�C
������������ݵ��ӵĵ�ʧ�غ��֪��1mol Cu������ϡ���ᷴӦ����2NA/3��NO���ӣ�ѡ��C����ȷ����״���£�CHCl3�������壬��������������Ħ��������������ӵĻ�ԭ�����ڵ����ӵģ�������������������ǵ����ӣ�����ѡ��D���ܹ�ת�Ƶ��ӵ���ĿΪ3 NA�������ȷ�Ĵ�ѡC��
�����Ѷȣ�����
5��ѡ���� �ڳ��³�ѹ�£���100mLCH 4��Ar�Ļ��������ͨ��400mLO2����ȼʹ����ȫ��Ӧ���������ͬ�����µõ���������450mL����Ӧǰ���������CH4��Ar�����ʵ���֮��Ϊ
A��1:4
B��1:3
C��1:2
D��1:1
�ο��𰸣�B
������������ݷ���ʽ�����ó�������ȫ��Ӧ������ʣ�࣬���У�
CH4+2O2=CO2+2H2O? ��V
1? 3-1
n? 500-450
n=50��2=50mL
���������CH4��Ar�����ʵ���֮��Ϊ50:150=1��3
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���������й�������.. | |
| �����Ŀ |