��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����װ���Ƿ��չ�ҵ���Ʊ�����Ĺ���������Ƴ����ģ�����̽����ҵ��Ϊ�β���98.3%��Ũ����������������

��ش��������⣺
��1��д������¯�����ջ�����Ļ�ѧ����ʽ______��
��2����ͼ�е��ҡ����ֱ��൱�ڹ�ҵ����ȡ�����豸�е�______��______��
��3�����е�����Ϊ______��
��4����ͼ��ѹǿ��SO2ƽ��ת���ʵ�Ӱ�죺
| ת����%? ѹǿ/MPa? �¶�/�� | 0.1 | 0.5 | 1 | 10
400
99.2
99.6
99.7
99.9
500
93.5
96.9
97.8
99.3
600
73.7
85.8
89.5
96.4
|
��SO2ת��ΪSO3�ķ�Ӧ������ѹǿ��ʹת����______����ҵ������ͨ�����ó�ѹ������ԭ����______��
�ο��𰸣���1����ҵ�Ӵ��������������裺��һ����SO2����ȡ���ڶ�����SO3����ȡ������������������ɣ���һ���ǻ������ȼ�գ���ѧ����ʽΪ4FeS2+11O2?����?.?2Fe2O3+8SO2��
�ʴ�Ϊ��4FeS2+11O2?����?.?2Fe2O3+8SO2��
��2��װ�����ǰ����ɵĶ���������������൱�ڹ�ҵ����ȡ�����豸�еĽӴ��ң�װ�ñ��൱�ڹ�ҵ����ȡ�����豸�е����������ʴ�Ϊ���Ӵ��ң���������
��3����ҵ��������������������98.3%��Ũ���ᣬ��ˮ���������γ�����Ӱ������Ч�����ʴ�Ϊ����������
��4����ҵ������2SO2��g��+O2��g���T2SO3��g������H=-98.3kJ?mol-1��Ӧ�Ʊ�SO3���÷�ӦΪ���淴Ӧ��������Ϊ������ٵķ��ȷ�Ӧ���ӻ�ѧƽ���ƶ���������Ӧ�ò��õ��¸�ѹ����������������������ѹǿ����ʹ���������ת�����������ݱ������ṩ�����ݷ��֣�ѹǿ����������SO2ת���ʵı仯�������ԣ����Թ�ҵ��ֱ�Ӳ��ó�ѹ��ͬʱ��Ӧ��ʹ�ô�����Ϊ��ʹ�����Ĵ�������ǿ�����ݱ������ṩ������Ӧ�ò���400�桫500�棻�ʴ�Ϊ������ѹ��SO2��ת�����Ѻܴ�
���������
�����Ѷȣ�һ��
2��ѡ���� һ�������£������Ϊ3L���ܱ������У�������ӦCO(g)+2H2(g)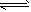 CH3OH(g)���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ����
CH3OH(g)���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ����
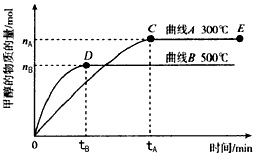
[? ]
A. ƽ�ⳣ��K(300��)<K(500��)
B. 300�棬��������ѹǿ����ʱ˵����Ӧ�Ѿ��ﵽƽ��
C. �������������������£��Դ���E�����ϵ���ѹ����ԭ����1/2��������Ũ�ȼ�С
D. 500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����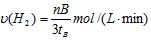
�ο��𰸣�B
���������
�����Ѷȣ�һ��
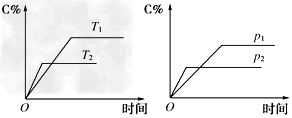
3��ѡ���� ��ӦaA(g)��bB(g)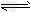 cC(g)����H��Q?kJ/mol��������C������������ѹǿp���¶ȵĹ�ϵ����ͼ������ʽ�еĻ�ѧ��������Qֵ����ͼ�����
cC(g)����H��Q?kJ/mol��������C������������ѹǿp���¶ȵĹ�ϵ����ͼ������ʽ�еĻ�ѧ��������Qֵ����ͼ�����
[? ]
A��a+b<c��Q>0������������
B��a+b>c��Q<0
C��a+b<c? Q<0?
D��a+b=c��Q>0
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪��4NH3(g)+5O2(g)=4NO(g)+6H2(g) ��H=-1025kJ/mol���÷�Ӧ��һ�����淴Ӧ������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����
[? ]
A. 
B. 
C. 
D. 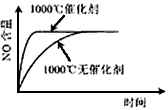
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5��ѡ���� ���ݻ��̶����ܱ������д������·�Ӧ��A ��g��+3B��g�� 2C��g������H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ
2C��g������H��0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ
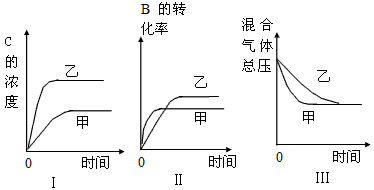
�����ж�һ���������
[? ]
A.ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬����ʹ�ô�����Ч�ʽϸ�
B.ͼ���о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ�
C.ͼ���о������¶ȶԷ�Ӧ��Ӱ�죬�Ҽ��¶Ƚϸ�
D.ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�ô�����Ч�ʽϸ�
�ο��𰸣�AB
���������
�����Ѷȣ�һ��