微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是____________晶体,31g白磷与足量的氧气完全燃烧释放出745.5kJ的热量,请写出白磷燃烧的热化学反应方程__________________________
(2)已知白磷和氯酸溶液可发生如下反应:
①____P4 +____HClO3+____ →___HCl +___H3PO4配平并完成上述反应方程式;
→___HCl +___H3PO4配平并完成上述反应方程式;
②该反应的氧化剂是______________。
参考答案:(1)分子;P4(s)+5O2(g) ===2P2O5(s);△H=-2982kJ/mol
(2)①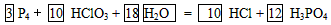 ;②HClO3
;②HClO3
本题解析:
本题难度:一般
2、计算题 氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) Fe3O4(s)+4H2(g) △H=akJ/mol (I)
Fe3O4(s)+4H2(g) △H=akJ/mol (I)
2Fe3O4(s) 6FeO(s)+O2(g) △H=bkJ/mol (II)
6FeO(s)+O2(g) △H=bkJ/mol (II)
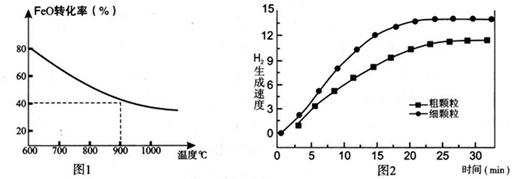
下列坐标图分别表示FeO的转化率(图-1 )和一定温度时,H2出生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图-2)。
(1)反应:2H2O(g)=2H2(g)+O2(g) △H= (用含a、b代数式表示);
(2)上述反应b>0,要使该制氢方案有实际意义,从能源利用及成本的角度考虑,实现反应II可采用的方案是: ;
(3)900°C时,在两个体积均为2.0L密闭容器中分别投人0.60molFeO和0.20mol H2O(g)甲容器用细颗粒FeO、乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②细颗粒FeO时H2O(g)的转化率比用粗颗粒FeO时H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计箅过程,保留两位有效数字)。
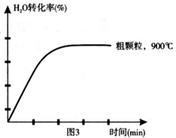
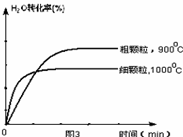
(4)在下列坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注)。
参考答案:(16分)(1)(2a+b)kJ/mol(2分)(无kJ/mol或“2a+b kJ/mol”扣1分,其他不给分)
(2)用廉价的清洁能源供给热能(2分)(答用“太阳能”、“风能”、“地热能”、“生物能”、“核能”供给热能给3分;答“加热”、“升高温度”等均不给分)
(3)①细颗粒FeO表面积大,与H2的接触面积大,反应速率加快(3分) (“增大接触面积,加快反应速率”、“接触面积越大,反应速率越快”等合理表述给3分;答“增大反应物浓度”、“FeO的量增加,反应速率加快”给1分); ②相等(2分)(答“等于”、“=”给1分)
③(4分)解:900℃时,达到平衡时FeO转化的量为:n(FeO)=0.60mol×40%=0.24mol
H2O(g)+3FeO(s) Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
起始物质的量(mol) 0.20 0.60 0 0
变化物质的量(mol) 0.080 0.24 0.080 0.080
平衡物质的量(mol) 0.12 0.36 0.080 0.080 (2分)
由于固体物质的浓度是常数,不能写入平衡常数表达式,气体物质的浓度可以变化,根据c=n/V可求平衡时氢气和水蒸气的物质的量浓度,则K=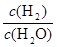 =
=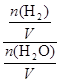 =
=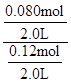 =0.67(2分)
=0.67(2分)
(4)(3分)
本题解析:(1)先对已知热化学方程式编号为①②,观察发现①×2+②可得,2H2O(g)=2H2(g)+O2(g),其焓变=①的焓变×2+②的焓变=(2a+b)kJ/mol;(2)b>0,说明反应II是吸热反应,可用用廉价的清洁能源供给热能或用“太阳能”、“风能”、“地热能”、“生物能”、“核能”供给热能;(3)①FeO是反应I中的固体反应物,细颗粒FeO表面积大,与H2的接触面积大,反应速率加快(或“增大接触面积,加快反应速率”、“接触面积越大,反应速率越快”等);②由于固体物质浓度是常数,FeO的用量和浓度保持不变,将粗颗粒FeO改为细颗粒FeO,只能加快反应速率,不能使平衡移动,因此H2O(g)的平衡转化率不变或相等;③解:900℃时,达到平衡时FeO转化的物质的量量为:n(FeO)=0.60mol×40%=0.24mol,则:
H2O(g)+3FeO(s) Fe3O4(s)+4H2(g)
Fe3O4(s)+4H2(g)
起始物质的量(mol) 0.20 0.60 0 0
变化物质的量(mol) 0.080 0.24 0.080 0.080
平衡物质的量(mol) 0.12 0.36 0.080 0.080
由于固体物质的浓度是常数,不能写入平衡常数表达式,气体物质的浓度可以变化,根据c=n/V可求平衡时氢气和水蒸气的物质的量浓度,则K=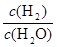 =
=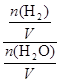 =
=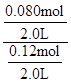 =0.67;
=0.67;
(4)观察图1可得:随着温度的升高,FeO的平衡转化率减小,前者导致平衡向吸热方向移动,后者说明平衡向逆反应方向移动,因此逆反应是吸热反应,则反应I的正反应是放热反应;其他条件保持不变时,900℃→1000℃就是升高温度,既能加快反应速率,又能使平衡向逆反应方向移动,则H2O(g)的转化率由0逐渐增大,知道达到平衡,1000℃时达到平衡的时间比900℃时少,1000℃时H2O(g)的平衡转化率比900℃时小,由此可以画出水蒸气的转化率随温度变化的示意图。
考点:考查化学反应原理,涉及盖斯定律、常见的能量转化形式、固体反应物颗粒粗细对反应速率和平衡移动的影响、化学平衡常数的计算、温度对反应速率和平衡移动的影响图像等。
本题难度:困难
3、填空题 “温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母)。
a.采用节能技术,减少化石燃料的用量 b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl="+1411.0" kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2="+1366.8" kJ/mol
则由乙烯水化制乙醇的热化学方程式是 。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。

根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率 (填“增大”“减小”或“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
参考答案:(1)abc(2分)(2)C2H4(g)+H2O(l)=C2H5OH(l) △H="-44.2" kJ/mol(2分)
(3)①增大(2分)②放(2分)
本题解析:(1)a.采用节能技术能减少化石燃料的使用,减少化石燃料的使用就减少了二氧化碳的排放,正确;b.化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;c.利用太阳能、风能能减少化石燃料的使用,化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;故选abc。
(2)2CO2(g)+2H2O(l)
本题难度:困难
4、填空题 (11分)应用化学学科知识,回答下列问题
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。已知在常温常压下:
2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) △H = -1275.6 kJ/mol
2CO(g)+O2(g)=2CO2(g) △H = -566.0 kJ/mol
H2O(g)=H2O(1) △H = -44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为 ________。
(2)水煤气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g) + CO(g)  CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g) △H=" +" 181.6KJ/mol。此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
物质
| H2
| CO
| CH3OH
|
浓度/(mol・L-1)
| 0.2
| 0.1
| 0.4
|
比较此时正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”)。
(3)已知A和B在一定条件下可建立如下平衡:2A(g)+B(g)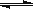 2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
2C(g)。在500℃时,分别将2 molA和1molB置于恒压容器Ⅰ和恒容容器Ⅱ中(两容器起始容积都为10L),充分反应。
①达到平衡所需时间是Ⅰ Ⅱ(填“>”、“<”或“=”,下同)。达到平衡后,两容器中C的体积分数关系是Ⅰ Ⅱ。
②平衡时,测得容器Ⅱ中的压强减小了30%,则该容器中A的转化率为 。
参考答案:(1)CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H =" -442.8" kJ/mol(3分)
(2) > (2分) (3) ①< (2分) >(2分) ② 90%(2分)
本题解析:(1)根据盖斯定律,将已知反应(①-②+③×4)÷2得到CH3OH(l)+O2(g)=CO(g)+2H2O(l),所以该反应的△H=[(-1275.6kJ/mol)-(-566.0kJ/mol)-(-44.0kJ/mol)×4]÷2=442.8kJ?mol-1,即CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ?mol-1。
(2)由表中数据可知,平衡时时氢气的浓度为0.2mol/L、CO的浓度为0.1mol/L、甲醇的浓度为0.4mol/L,则此时的浓度商Qc= =100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆。
=100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆。
(3)①平衡:2A(g)+B(g) 2C(g),是一个反应后气体系数和减小的反应,所以恒容容器下,反应达到平衡状态,恒压容器中随反应进行,为保持恒压,压强增大,达到平衡所需时间少,平衡正向移动,CO2的体积分数增大,CO2的体积分数关系是,恒压容器I大于恒容容器。
2C(g),是一个反应后气体系数和减小的反应,所以恒容容器下,反应达到平衡状态,恒压容器中随反应进行,为保持恒压,压强增大,达到平衡所需时间少,平衡正向移动,CO2的体积分数增大,CO2的体积分数关系是,恒压容器I大于恒容容器。
②在500℃时,分别将2mol A和1mol B置于恒容容器Ⅱ中(两容器起始容积都为10L),设A消耗物质的量为x 2A(g)+B(g) 2C(g)
2C(g)
起始量(mol) 2 1 0
变化量(mol) x 0.5 x x
平衡量(mol) 2-x 1-0.5x x
容器Ⅱ中的压强减小了30%,气体物质的量减小30%
3-3×30%=2-x+1-0.5x+x
X=1.8mol
A的转化率=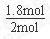 ×100%=90%。
×100%=90%。
考点:考查盖斯定律的应用、化学平衡计算以及外界条件对平衡状态的影响等
本题难度:困难
5、选择题 下列有关热化学方程式的评价合理的是( ? )
| ? | 实验事实 | 热化学方程式 | 评价
A | 已知H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1,将稀硫酸与 稀氢氧化钡溶液混合 | H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)
△H=-114.6 kJ?mol-1 | ?
正确
B | 稀醋酸与稀氢氧化钠溶液混合 | CH3COOH(aq)+NaOH(aq)=NaCl(aq)+H2O(l)
△H=-57.3k J?mol-1 | 不正确;因为醋酸状态为“l”,而不是“aq”.
C | 160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ | SO3(g)+H2O(l)=H2SO4(aq)△H=-130.3 kJ?mol-1 | 不正确;因为反应热为△H=-260.6 kJ?mol-1
D | 已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ | C(s)+O2(g)=CO2(g)
△H=-393.51 kJ?mol-1 | 不正确;同素异形体要注名称:C(石墨,S)
|