��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и������ʣ���ѧ��������ͬ������������ͬ���ۻ�ʱ�ƻ�����������Ҳ��ͬ����
A.NaOH Na2O2
B.H2S CCl4
C.NH4Cl KCl
D.CO2 SiO2
�ο��𰸣�B
������������������B�У�H2S��CCl4�Ļ�ѧ�����Ͷ�Ϊ���ۼ��������������Ͷ�Ϊ���Ӿ��壬�ۻ�ʱ�ƻ��������������ڷ��Ӽ������������Դ�ΪB��
���㣺��ѧ�����͡���������
���������⿼��Գ������ʻ�ѧ�����͡��������͵��жϣ��Ǹ߿������Ŀ��㣬���⿼��Ķ��dz�����֪ʶ�㣬�Ƚ����ס�
�����Ѷȣ�����
2��ѡ���� ���������в���ͨ�������뵥��ֱ�ӷ�Ӧ���ɵ���
A.Na2O
B.FeCl2
C.NO
D.SiO2
�ο��𰸣�B
����������������������ʵ����ʽ����жϣ�������������ǿ�����ԣ�����������Ӧֻ���ϴ��Ȼ������������ʿ��ɵ���ֱ�����ɣ�
���A��Na��O2�ڲ����������¿ɷ�Ӧ����Na2O����A��ѡ��
B������������Ӧֻ���ϴ��Ȼ�������Bѡ��
C�������ڷŵ������¿���������Ӧ����NO����C��ѡ��
D��Si��������ֱ�ӷ�Ӧ����SiO2����D��ѡ��
��ѡB��
���������⿼��Ԫ�ػ�����֪ʶ�������ڻ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ���ע�ⳣ�����ʵķ�Ӧ�ص�����ʣ�
�����Ѷȣ���
3��ѡ���� ���������У������Լ��ͷǼ��Լ��ҷ����м��Ե���
A.��ϩ
B.��ȩ
C.�״�
D.���ȼ���
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� 1.7�˻�����H2A����3.01��1022��H2A���ӣ���H2A����Է�������Ϊ
A.17
B.34
C.16
D.32
�ο��𰸣�B
�����������������ͨ���������������ʵ������ٸ������������ʵ����Ĺ�ϵ����Ħ��������Ħ����������ֵ��������Է���������ȣ��Ӷ��ó���Է���������
��𣺸���N=n��NA ��n�T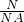 �T=
�T=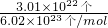 =0.05mol��
=0.05mol��
����m=n��M��M=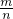 =
=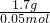 =34g/mol��
=34g/mol��
Ħ����������ֵ��������Է���������ȣ���������Է���������34��
��ѡB
���������⿼������й����ʵ����ļ��㣬����Ҫ��ס������ʽ��Ҫ���Ƶ����������ʵ�������������������Ħ������֮��Ĺ�ϵ�ǽ���Ĺؼ�������ʱҪϸ�ģ�ע�����и������Ƿ���������ԭ������������ȷ���
�����Ѷȣ�����
5��ѡ���� 100mL?0.3mol/L?Na2SO4��Һ��50mL?0.2mol/L?Al2��SO4��3��Һ��Ϻ���Һ��SO42-�����ʵ���Ũ��ԼΪ
A.0.20mol/L
B.0.25mol/L
C.0.4mol/L
D.0.5mol/L
�ο��𰸣�C
����������������ֱ����100mL?0.3mol/L?Na2SO4��Һ��50mL?0.2mol/L?Al2��SO4��3��Һ��SO42-�����ʵ����������ʵ���������Һ�������������Һ��SO42-�����ʵ���Ũ�ȣ�
���100mL?0.3mol/L?Na2SO4��Һ��SO42-�����ʵ���Ϊ0.1L��0.3mol/L=0.03moL��
50mL?0.2mol/L?Al2��SO4��3��Һ��SO42-�����ʵ���Ϊ0.05L��0.2moL/L��3=0.03mol��
��Ϻ����SO42-�����ʵ���Ϊ0.03moL+0.03moL=0.06mol��
��Һ��Ϻ���Һ��SO42-�����ʵ���Ũ��Ϊ�� =0.4mol/L��
=0.4mol/L��
��ѡC��
���������⿼�����ʵ���Ũ�ȵļ��㣬��Ŀ�ѶȲ�����ע����Һ��Ϻ������ʵ���������Һ�������������Һ��SO42-�����ʵ���Ũ�ȣ�
�����Ѷȣ���