微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应中,既属于氧化还原反应又属于置换反应的是
A.H2+CuO△ Cu+H2O
B.Ca(OH)2+CO2 =CaCO3↓+H2O
C.3CO+Fe2O3高温2Fe+3CO2
D.4Al+3O2 点燃2Al2O3
参考答案:A
本题解析:氧化还原反应的判断方法是看反应前后有无元素化合价的变化,置换反应是单质与化合物反应生成另一种单质和另一种化合物,结合此可以确定选A。B两个都不是,C不是置换反应,D不是置换反应。所以答案选A。
本题难度:简单
2、选择题 现有常温下的四份溶液:① 0.01mol/LCH3COOH;② 0.01mol/LHCl;③ pH=12的氨水;④ pH=12的NaOH溶液。下列说法正确的是
A.①中水的电离程度最小,②③④中水的电离程度一样大
B.将②③混合,若pH=7,则消耗溶液的体积:②<③
C.将①、④混合,若有c(CH3COO?)>c(H+),则混合液一定呈碱性
D.将①、④等体积混合,所得溶液中一定有:c(OH?)=c(H+) + c(CH3COOH)
参考答案:D
本题解析:试题分析:A、酸碱抑制水的电离,CH+或COH-越大,水的电离程度越小。水的电离程度:③最小,②④相近,①最大。错误;B、将②③混合,若pH=7,则消耗溶液的体积:②>③。因为氨水是弱电解质,浓度大,则消耗溶液的体积小。错误;C、未给定体积,若CH3COOH过量,则混合液呈酸性;若恰好反应或碱过量,则混合液一定呈碱性。错误;D、将①、④等体积混合,得CH3COONa,由质子守恒得c(OH?)=c(H+) + c(CH3COOH),正确。
考点:考查溶液里的离子浓度比较等相关知识。
本题难度:一般
3、选择题 下列说法正确的是
A.凡是同种分子构成的物质都是纯净物
B.含有氧元素的化合物是氧化物
C.同种元素组成的物质一定是单质
D.质子数相同的微粒,一定属于同种元素
参考答案:A
本题解析:
本题难度:简单
4、填空题 (8分)水是生命之源,也是化学反应中的主角。试回答下列问题:
(1)写出水分子的结构式 。
(2)全部由短周期元素组成的A、B、C三种物质,是中学化学常见的有色物质,它们均能与水发生氧化还原反应,但反应中水既不作氧化剂也不作还原剂。请写出A、B、C与水反应的化学方程式:
①A十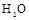 __________________ _______ __;
__________________ _______ __;
②B十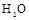 ;
;
③C十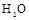 。
。
参考答案:(共8分)(1)H-O-H(2分)
(2)①3NO2+H2O=2HNO3+NO ②Cl2+H2O=HCl+HClO③2Na2O2+2H2O=4NaOH+O2↑(每个2分,共6分;以上答案顺序可填倒)
本题解析:(1)水是由极性键形成的共价化合物,结构式是H-O-H。
(2)满足条件的三种有色物质分别是氯气、NO2和过氧化钠,因此和水反应的方程式分别是3NO2+H2O=2HNO3+NO、Cl2+H2O=HCl+HClO、2Na2O2+2H2O=4NaOH+O2↑。
本题难度:一般
5、选择题 常温下有0.1mol・L-1的NaHA溶液,其pH=9,下列说法正确的是
A.c(Na+)=c(HA-)+c(A2-)+c(H2A)
B.c(HA-)>c(Na+)>c(OH-)>c(H+)
C.c(Na+)>c(HA-)>c(OH-)>c(H2A)
D.c(H+)+2c(H2A)= c(OH-) +c(A2-)
参考答案:AC
本题解析:试题分析:由于NaHA=Na++HA-,H2O=H++OH―,HA-+H2O=H2A+OH―,HA-=H++A2―,则平衡时溶液中的HA-、H2A、A2―均来自原料中的NaHA,根据物料守恒原理可得:c(Na+)=c(HA-)+c(A2-)+c(H2A),故A选项正确;由于溶液的pH=9,说明该盐是强碱弱酸盐,Na+不能水解,HA-既能微弱地水解,也能微弱的电离,且水解程度大于其电离程度,因此平衡时溶液中c(Na+)>c(HA-)>c(OH-)>c(H+),故B选项错误;由于盐电离出的HA-具有两性,则水电离出的氢离子部分与HA-反应生成H2A,即H++ HA-=H2A,该反应中H2A与H+的系数之比等于浓度之比,则被消耗的氢离子浓度等于生成的H2A的浓度,即c(H+)水= c(H+)+c(H2A),而水电离出的部分氢氧根离子与HA-中和生成水和A2―,即OH―+HA-= A2―+H2O,该反应中A2―与OH―的系数之比等于浓度之比,则被消耗的氢氧根离子浓度等于生成的A2―的浓度,即c(OH-)水= c(OH-)+c(A2―),由于水电离出的氢离子等于水电离出的氢氧根离子,则平衡时溶液中c(H+)+c(H2A)=c(OH-)+c(A2―),故D选项错误;由于溶液的pH=9,则c(H+)=10―9mol/L,由于常温下水的离子积为1.0×10―14,c(OH-)=Kw/ c(H+)=10―5mol/L,则c(H+)< c(OH-),由于HA-的水解程度大于其电离程度,则其水解产物浓度大于电离产物浓度,则c(H2A)> c(A2―),由于质子守恒关系式为c(H+)+c(H2A)=c(OH-)+c(A2―),则c(H2A)<c(OH-),由于钠离子不能水解,HA-既能微弱地水解,也能微弱的电离,则c(Na+)>c(HA-)>c(OH-)>c(H2A),故C选项正确。
考点:考查考生对溶液pH的了解;考查考生对水的电离和离子积常数的了解;考查考生对盐在水中的水解平衡的了解;考查考生对水溶液中离子浓度大小的比较;考生对物料守恒原理、质子守恒原理的了解。
本题难度:困难