微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在硫酸铁溶液中,加入a g铜,完全溶解后,又加入b g铁,充分反应后得到c g残余固体,且b<c,则下列判断正确的是? ( )
A.最后得到的溶液中含有Fe3+
B.残余固体可能为铁、铜混合物
C.最后得到的溶液中只含Cu2+
D.残余固体一定全部是铜
参考答案:B
本题解析:试题分析:本题涉及的反应有:(1)Cu+2Fe3+==Cu2++2Fe2+,(2)Fe+Cu2+==Fe2++Cu,所以C不正确;由于题目中b<c,说明所加的Fe的量不确定,若Fe的量不足,说明Cu没有被全部置换出来,Cu2+ 没有完全反应掉,故残留固体全部为Cu;若Fe过量,且符合b<c,则残余固体可能为铁、铜混合物,所以B正确,D不正确;因为Fe3+能够氧化Cu,所以当残留固体中有Cu存在时,溶液中一定不含有Fe3+,所以A不正确。故选B。
考点:铁及其化合物的知识
点评:本题主要考查铁及其化合物的知识,要求会判断反应物与产物,题目难度中等。
本题难度:一般
2、选择题 若100 mL 0.1 mol・L-1硫酸铝溶液与氢氧化钠溶液反应,得到1.17g沉淀,则需0.5 mol・L-1NaOH溶液
A.130mL
B.100mL
C.90mL
D.50mL
参考答案:AC
本题解析:设所需NaOH溶液的体积为V。
若Al3+过量:
Al3++3OH- Al(OH)3↓
Al(OH)3↓
3 mol? 78 g
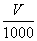 ×0.5 mol・L-1?1.17 g
×0.5 mol・L-1?1.17 g
解得V="90" mL。
若OH-过量:
Al3+ + 3OH-? Al(OH)3↓
Al(OH)3↓
1mol ?3 mol? 78 g
0.02 mol ?0.06 mol 1.56 g
Al(OH)3+ OH-?![]()
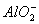 +2H2O
+2H2O
78 g?1 mol
(1.56-1.17)g ?0.005 mol
则: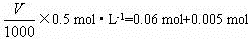
V=130mL。
本题难度:简单
3、选择题 关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可能确定有Cl-存在
B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I一存在
C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有SO42-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在
参考答案:B
本题解析:分析:A、稀盐酸沉淀时,HCl中含有大量Cl-离子,所以不能确定Cl-离子是原溶液里的还是后来加进去的;
B、氯气具有氧化性,能将碘离子氧化;
C、亚硫酸钡白色沉淀可以被硝酸氧化为硫酸钡;
D、碳酸根和碳酸氢跟能和氢离子反应生成水和二氧化碳.
解答:A、因加HCl之前生成的可能是AgCl沉淀,也可能是别的白色沉淀,但是后面加上HCl中含有大量Cl-离子,所以不能确定Cl-离子是原溶液里的还是后来加进去的,故A错误;
B、氯气具有氧化性,能将碘离子氧化为碘单质,碘水呈黄色,碘单质遇到淀粉变蓝色,故B正确;
C、因为加入的是硝酸钡,溶液中存在了硝酸根离子,再加入盐酸时引入氢离子,就相当于存在了硝酸,将亚硫酸根离子氧化为硫酸根离子,与钡离子形成不可溶的硫酸钡沉淀,也可能含有亚硫酸离子,故C错误;
D、能和盐酸反应生成能使澄清石灰水变浑浊的二氧化碳气体的可以是碳酸根、碳酸氢根等离子,此外二氧化硫也能使石灰水变浑浊,故D错误.
故选B.
点评:本题强调的A选项,原因是别的白色沉淀加上HCl转化为AgCl沉淀,这一点需要特别注意,容易出错.
本题难度:简单
4、选择题 某溶液中存在较多的H+、SO42-、NO3-,则该溶液中还可能大量存在的离子组是
A.Mg2+、NH4+、Cl-
B.Mg2+、Ba2+、Br-
C.Na+、Cl-、I-
D.Al3+、HCO3-、Cl-
参考答案:A
本题解析:试题分析:A中的离子可以和溶液中的H+、SO42-、NO3-共存;B中Ba2+溶液中SO42-形成沉淀;C中Cl-、I-会被溶液中的硝酸氧化;D中的HCO3-和溶液中的H+反应,不能共存。
考点:离子共存
本题难度:简单
5、选择题 将0.1mol无水硫酸铜固体于强热下完全分解,得到Cu2O与SO3、SO2、O2的混合气体,该混合气体的平均式量 可能为
A.32
B.48
C.64
D.72
参考答案:C
本题解析:分析:CuSO4分解得到Cu2O、SO3、SO2、O2,根据质量守恒定律可知,混合气体的总质量一定,利用硫原子守恒可知,硫的氧化物的物质的量之和为0.1mol,故混合气体的平均式量取决于氧气的物质的量,反应中铜元素的化合价降低,一定会有元素化合价升高,一定有氧气生成,利用极限法分析,根据电子转移守恒可知,当产生的气体为SO3和O2时,O2的物质的量最小,混合气体的物质的量最小,平均式量最大;产生的气体为O2和SO2时,O2的物质的量最大,混合气体的物质的量最大,平均式量最小;
根据铜原子守恒计算Cu2O的物质的量,再根据m=nM计算Cu2O的质量,进而计算混合气体的物质的量,根据极限法,利用电子转移守恒计算氧气的物质的量,进而计算平均式量的极值,据此判断.
解答:CuSO4分解得到Cu2O、SO3、SO2、O2,根据质量守恒定律可知,混合气体的总质量一定,利用硫原子守恒可知,硫的氧化物的物质的量之和为0.1mol,故混合气体的平均式量取决于氧气的物质的量;
根据铜原子守恒可知,n(Cu2O)=0.05mol,故m(Cu2O)=0.05mol×144g/mol=7.2g,
故混合气体的质量为:0.1mol×160g/mol-7.2g=8.8g,
反应中铜元素的化合价降低,一定会有元素化合价升高,一定有氧气生成,根据电子转移守恒可知:
①当产生的气体为SO3和O2时,O2的物质的量最小,混合气体的物质的量最小,平均式量最大,由电子转移守恒可知,此时O2的物质的量为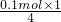 =0.025mol,由硫原子守恒可知n(SO3)=0.1mol,故混合气体的平均式量最大值为
=0.025mol,由硫原子守恒可知n(SO3)=0.1mol,故混合气体的平均式量最大值为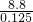 =70.4;
=70.4;
②当产生的气体为O2和SO2时,O2的物质的量最大,混合气体的物质的量最大,平均式量最小,由硫原子守恒可知n(SO2)=0.1mol,由电子转移守恒可知,此时O2的物质的量为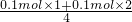 =0.075mol,故混合气体的平均式量最小值为
=0.075mol,故混合气体的平均式量最小值为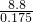 =50.3;
=50.3;
由于实际混合气体是SO3、SO2、O2三种气体的混合气体,故其平均式量应该在50.3~70.4之间,
故选C.
点评:本题考查混合物的有关计算,难度中等,注意利用极限法确定极值进行解答,关键是确定混合气体物质的量的极值.
本题难度:一般