��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��13�֣���1�������£�0.05mol/L������Һ��,c(H+)=?mol/L��pHֵΪ?��ˮ�����c(H+)=?mol/L����ͼ��ʾ��һ���¶��£��������ˮϡ��������Һ�ĵ�����������ͼ����ش�

��2����O����Ϊʲô������?��
��3��a��b��c�����������Ũ����С�����˳��Ϊ?��
��4��a��b��c�����У�����ĵ���̶�����һ����?��
��5����ʹc����Һ�е�c(CH3COO��)��ߣ������´�ʩ�У���ѡ��?��
A����NaCl��Һ?B������?
C���ӹ���KOH?D����Zn��
E���ӹ���CH3COONa ? F����ˮ
��6����ϡ�����У����Ŵ���Ũ�ȵĽ��ͣ�����ʼ�ձ����������Ƶ�����__________________��
A.H������?B��c(H��)
C��c(H��)/c(CH3COOH)? D��CH3COOH������
�ο��𰸣���1��0.1 mol/L? 1? 10-13 mol/L?��2����Ϊ������δ���룬�������ƶ�������
��3��c<a<b��?��4��c��?��5��B��C��D��E?��6��A��C
�����������1��0.05mol/L������Һ��c(H+)=0.1 mol/L��pHֵΪ1��ˮ�����c(H+)Ϊ10-13 mol/L��
��2����O�����û�е��룬ֻ�д�����ӣ��������ƶ������ӣ����Բ��ܵ��硣
��3��������Ũ��Խ��������Խǿ�����Ը���ͼ���֪������Ũ�ȵĴ�С˳��Ϊb>a>c��
��4�����������ᣬ���ڵ���ƽ�⣬ϡ�ʹٽ����룬����c�����ĵ���̶����
��5������CH3COOH CH3COO����H+����NaCl��Һ��ƽ�ⲻ�ƶ�c(CH3COO��)���䣬����ƽ�������ƶ���c(CH3COO��)���ӹ���KOH��ƽ�������ƶ���c(CH3COO��)����Zn����ƽ�������ƶ���c(CH3COO��)���ӹ���CH3COONa��ƽ�������ƶ�����c(CH3COO��)����ˮƽ�������ƶ�����c(CH3COO��)��С��������ʹc(CH3COO��)����Ĵ�ʩ��BCDE��
CH3COO����H+����NaCl��Һ��ƽ�ⲻ�ƶ�c(CH3COO��)���䣬����ƽ�������ƶ���c(CH3COO��)���ӹ���KOH��ƽ�������ƶ���c(CH3COO��)����Zn����ƽ�������ƶ���c(CH3COO��)���ӹ���CH3COONa��ƽ�������ƶ�����c(CH3COO��)����ˮƽ�������ƶ�����c(CH3COO��)��С��������ʹc(CH3COO��)����Ĵ�ʩ��BCDE��
��6������CH3COOH CH3COO����H+��ϡ������ƽ�������ƶ���H���������ӣ�c(H��)��С��c(CH3COO��)��С��CH3COOH��������С������K=
CH3COO����H+��ϡ������ƽ�������ƶ���H���������ӣ�c(H��)��С��c(CH3COO��)��С��CH3COOH��������С������K=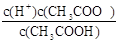 ��c(CH3COO��)��С������
��c(CH3COO��)��С������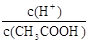 �������ѡAC��
�������ѡAC��
�����������ۺ��Խ�ǿ���ѶȽϴ���ҪҪ���ú�ƽ�ⳣ����
�����Ѷȣ�һ��
2��ѡ���� ��ij��Һ�н��еķ�Ӧ��A+2B 3C���¶�ÿ����10�棬�䷴Ӧ��������ԭ����3������֪��20��ʱv(A��="0.1" mol��L-1��min-1,��������������ʱ�����¶����ߵ�40��ʱ����v(B��Ӧ����(?��
3C���¶�ÿ����10�棬�䷴Ӧ��������ԭ����3������֪��20��ʱv(A��="0.1" mol��L-1��min-1,��������������ʱ�����¶����ߵ�40��ʱ����v(B��Ӧ����(?��
A.0.6 mol��L-1��min-1? B.0.9 mol��L-1��min-1
C.1.2 mol��L-1��min-1? D.1.8 mol��L-1��min-1
�ο��𰸣�D
�����������Ϊ��Ӧ�и����ʱ�ʾ������֮�ȵ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȣ���v(A)��v(B)=1��2����֪����20��Cʱ��v(A)=0.1mol��L-1��min-1����v(B)="2��v(A)=2��" 0.1mol��L-1��min-1 =0.2mol��L-1��min-1��
�������⣬�䷴Ӧ������ÿ����10��C������ԭ����3�������Ե��¶ȴ�20��C���ߵ�40��Cʱ��v(B)Ӧ��0.2mol��L-1��min-1��32=1.8mol��L-1��min-1��
�����Ѷȣ���
3��ѡ���� ����˵���п���˵��2HI��g�� H2��g��+I2��g���Ѵﵽƽ��״̬���ǣ�?��
H2��g��+I2��g���Ѵﵽƽ��״̬���ǣ�?��
��1����λʱ��������n mol H2��ͬʱ����n mol HI
��2��һ��H��H�����ѵ�ͬʱ������H��I������
��3��c(HI)= c(I2)
��4����Ӧ���ʦ�(H2)=��(I2)=0.5��(HI)
��5��c(H2)��c(I2)��c(HI)=2��1��1
��6���¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯
��7���¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯
��8������һ������������ƽ����Է����������ٱ仯
��9���¶Ⱥ����һ��ʱ������������ɫ���ٷ����仯
��10���¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٷ����仯
�ο��𰸣���2����6����9��
����������жϿ��淴Ӧ�Ƿ��Ѵ�ƽ��״̬���ؼ��ǽ���Χ�����š��ȡ�[�ԣ��������ԣ��棩]�롰����������һ������Ӧ�����ĺ������ֲ��䣩�������������жϡ���������������ָ��Ӧ�����ĺ�������ȡ����ߡ��ɱ��������ر�Ӧ2HI H2+I2��g��������ļ�����ǰ�䡣��1����Ȼ��ʾ���Dz�ͬ�ķ�Ӧ��������֤���ԣ��������ԣ��棩���ʲ���ȷ����2���ܱ�ʾ�ԣ��������ԣ��棩���������ȷ����3������5����Ũ����Ȼ�ɱ�����������˵�����������������壬�ʲ���ȷ����4������֮����Ȼ��ȷ����δָ���������ʵĹ�ϵ���ʲ���ȷ����6������һ����ijһ������Ũ�Ȳ��ٱ仯��˵���ˡ��������������壬����ȷ����7�����ڷ�Ӧ2HI��g��
H2+I2��g��������ļ�����ǰ�䡣��1����Ȼ��ʾ���Dz�ͬ�ķ�Ӧ��������֤���ԣ��������ԣ��棩���ʲ���ȷ����2���ܱ�ʾ�ԣ��������ԣ��棩���������ȷ����3������5����Ũ����Ȼ�ɱ�����������˵�����������������壬�ʲ���ȷ����4������֮����Ȼ��ȷ����δָ���������ʵĹ�ϵ���ʲ���ȷ����6������һ����ijһ������Ũ�Ȳ��ٱ仯��˵���ˡ��������������壬����ȷ����7�����ڷ�Ӧ2HI��g�� H2��g��+I2��g����ǰ������������䣬���¶ȡ����һ��ʱ��ѹǿ���䲻��˵����Ӧ�Ѵ�ƽ��״̬�������ڷ�Ӧ2NO2
H2��g��+I2��g����ǰ������������䣬���¶ȡ����һ��ʱ��ѹǿ���䲻��˵����Ӧ�Ѵ�ƽ��״̬�������ڷ�Ӧ2NO2 N2O4��ǰ�������������ȣ����¶ȡ����һ��ʱ��ѹǿ������˵���κ����ʵ����ʵ������䣬Ϊ������ֵ���ʷ�Ӧ�Ѵ�ƽ��״̬����8�����ڷ�Ӧ2HI��g��
N2O4��ǰ�������������ȣ����¶ȡ����һ��ʱ��ѹǿ������˵���κ����ʵ����ʵ������䣬Ϊ������ֵ���ʷ�Ӧ�Ѵ�ƽ��״̬����8�����ڷ�Ӧ2HI��g�� H2��g��+I2��g����ǰ���������ʵ������䣬�������䣬��������ƽ����Է����������ٱ仯����˵����Ӧ�Ѵ�ƽ�⣻�����ڷ�Ӧ2NO2
H2��g��+I2��g����ǰ���������ʵ������䣬�������䣬��������ƽ����Է����������ٱ仯����˵����Ӧ�Ѵ�ƽ�⣻�����ڷ�Ӧ2NO2 N2O4��ǰ���������ʵ�������ȣ��������䣬��������ƽ����Է����������ٱ仯��˵���κ����ʵ����ʵ������䣬Ϊ������ֵ���ʷ�Ӧ�Ѵ�ƽ�⣻��9������������ɫ���ٷ����仯��˵�������ʵ�Ũ�Ȳ��䣬֤����Ӧ�Ѵ�ƽ��״̬����10�����ڷ�Ӧ2HI��g��
N2O4��ǰ���������ʵ�������ȣ��������䣬��������ƽ����Է����������ٱ仯��˵���κ����ʵ����ʵ������䣬Ϊ������ֵ���ʷ�Ӧ�Ѵ�ƽ�⣻��9������������ɫ���ٷ����仯��˵�������ʵ�Ũ�Ȳ��䣬֤����Ӧ�Ѵ�ƽ��״̬����10�����ڷ�Ӧ2HI��g�� H2��g��+I2��g����ǰ���������ʵ������䣬���¶ȡ�ѹǿһ��ʱ��������䣬�ܶȲ��䣬����˵����Ӧ�Ѵ�ƽ��״̬�������ڷ�Ӧ2NO2
H2��g��+I2��g����ǰ���������ʵ������䣬���¶ȡ�ѹǿһ��ʱ��������䣬�ܶȲ��䣬����˵����Ӧ�Ѵ�ƽ��״̬�������ڷ�Ӧ2NO2 N2O4��ǰ���������ʵ�������ȣ����¶ȡ�ѹǿһ��ʱ��������䣬�ܶȲ��䣬��˵����Ӧ�Ѵ�ƽ��״̬��
N2O4��ǰ���������ʵ�������ȣ����¶ȡ�ѹǿһ��ʱ��������䣬�ܶȲ��䣬��˵����Ӧ�Ѵ�ƽ��״̬��
�����Ѷȣ�һ��
4��ѡ���� ������һ�ܱ������н��е����з�Ӧ��C��s��+ O2��g�� CO2��g������˵���д������? (? )
CO2��g������˵���д������? (? )
A����ľ̿����ɷ�ĩ״���Լӿ컯ѧ��Ӧ����
B�������¶ȿ��Լӿ컯ѧ��Ӧ����
C���������������С��ԭ����һ�룬�����ʵ����ʵ�������, ��ѧ��Ӧ���ʲ���
D������ľ̿�������Լӿ컯ѧ��Ӧ����
�ο��𰸣�CD
���������ľ̿�ǹ��壬�ı����ı�������Լӿ췴Ӧ���ʣ�A��ȷ��ͬ�������¶ȷ�Ӧ�����Ǽӿ�ģ�B��ȷ���������������С��ԭ����һ�룬������ѹǿ��ƽ�ⲻ�ƶ�������Ӧ���ʼӿ죬C����ȷ���ı�������������Ӧ���ʲ��䣬D����ȷ����ѡCD��
������Ũ�ȶԷ�Ӧ���ʺ�ƽ��״̬��Ӱ�첻�������ڹ���ʹ�Һ�壻ѹǿ�Է�Ӧ���ʻ�ƽ��״̬��Ӱ��ֻ��������������μӻ����ɵģ���ʵ����ͨ���ı�Ũ������ġ�
�����Ѷȣ�һ��
5������� �о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ�������Ҫ���壮
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ����ʽΪ______�����÷�Ӧ
6NO2+8NH3
7N2+12H2OҲ���Դ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______L��
��2����֪��2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ?mol-1
2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
��ӦNO2��g��+SO2��g��?SO3��g��+NO��g���ġ�H=______kJ?mol-1
һ�������£����������1��2�����ܱ������з���������Ӧ��������˵����ӳ�ﵽƽ��״̬����______��
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1molSO3��ͬʱ����1molNO2
���������Ӧƽ��ʱ��NO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=______��
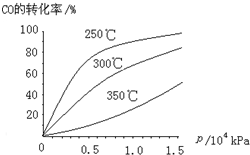
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO��g��+2H2��g��?CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ���÷�Ӧ��H______0���������������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ��������______��
�ο��𰸣���1��NO2��H2O��Ӧ�ķ���ʽΪ��3NO2+H2O�T2HNO3+NO��6NO2+8NH3�T7N2+12H2O������Ӧ����1 mol NO2�μӷ�Ӧʱ����ת����4 mol���ӣ���ת��1.2mol����ʱ�����ĵ�NO2Ϊ1.2��4��22.4L=6.72L��
��2�����ݸ�˹���ɣ����ڶ�������ʽ�ߵ����������һ������ʽ��ӵã�2NO2+2SO2�T2SO3+2NO����H=-83.6 kJ?mol-1����NO2+SO2?SO3+NO����H=-41.8 kJ?mol-1������Ӧ�Ƿ�Ӧǰ���������������ķ�Ӧ������ϵ��ѹǿ���ֲ��䣬��a����˵����Ӧ�Ѵﵽƽ��״̬�����ŷ�Ӧ�Ľ��У�NO2��Ũ�ȼ�С����ɫ��dz����b����˵����Ӧ�Ѵ�ƽ�⣻SO3��NO�����������������1��1����c������Ϊƽ��״̬���ж����ݣ�d���������������ʶ����淴Ӧ���ʣ�������Ϊƽ��״̬���ж����ݣ�
NO2��g��+SO2��g�� SO3��g��+NO��g��
SO3��g��+NO��g��
��ʼ���ʵ���� 1a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� 1a-x 2a-xxx
��1a-x������2a-x��=1��6����x=45a����ƽ�ⳣ��Ϊ=x2/��1a-x����2a-x��=8/3��
��3����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ������淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H��0��ѹǿ�������ڼӿ췴Ӧ���ʣ�������ʹƽ�������ƶ�����ѹǿ������Ҫ�Ķ������豸��Ҫ��Ҳ�ߣ���ѡ��250�桢1.3��104kPa���ҵ���������Ϊ��250�桢ѹǿΪ1.3��104 kPaʱ��CO��ת�����ѽϴ�������ѹǿ��CO��ת���ʱ仯����û�б�Ҫ������ѹǿ��
�ʴ�Ϊ����1��3NO2+H2O=2HNO3+NO��6.72
��2��-41.8��b��2.67��8/3
��3��������1.3��104kPa�£�CO��ת�����ѽϸߣ�������ѹǿCO��ת������߲��������ɱ����ӵò���ʧ��
���������
�����Ѷȣ�һ��