微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
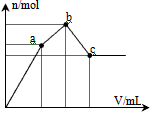
1、选择题 向100 mL 0.1 mol・L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol・L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
[? ]
A.a点对应的沉淀只有BaSO4
B.c点溶液呈碱性
C.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-==Al(OH)3↓+2BaSO4↓
D.c点加入Ba(OH)2溶液的体积为200 mL
参考答案:B
本题解析:
本题难度:一般
2、选择题 在实验室里,要想使AlCl3溶液中的Al3+全部沉淀出来 ,应选用下列试剂中的
[? ]
A.Ba(OH)2溶液
B.NaOH溶液
C.氨水
D.硫酸
参考答案:C
本题解析:
本题难度:一般
3、选择题 氨和酸反应生成铵盐的实质是
A.氨极易溶于水
B.氨具有碱性
C.氨分子与H+形成配位键
D.氨分子是极性分子
参考答案:C
本题解析:
本题难度:困难
4、填空题 (1)AlCl3溶液加热蒸干后灼烧所得固体是___________
(2)Al2(SO4)3溶液加热蒸干所得固体是_________ Al2(SO4)3水解的离子方程式为____________ 。
参考答案:(1)Al2O3?
(2) Al2(SO4)3?; Al3++3H2O 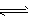 Al(OH)3+3H+
Al(OH)3+3H+
本题解析:
本题难度:一般
5、填空题 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题

(1)④、⑤、⑥的原子半径由大到小的顺序是_____________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________________。
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应
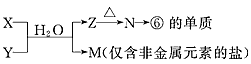
X溶液与Y溶液反应的离子方程式为______________________,N→⑥的单质的化学方程式为_________________________,常温下,为使0.1 mol/L M溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至___________。
参考答案:(1)Na>Al>O
(2)HNO3>H2CO3>H2SiO3(3)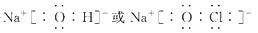 (4)ab
(4)ab
(5)Al3++3NH3・H2O==Al(OH)3↓+3NH4+;2Al2O3(熔融) 4Al+3O2↑;溶液的pH等于7
4Al+3O2↑;溶液的pH等于7
本题解析:
本题难度:一般