微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是
A.可用于电动汽车的铝-空气燃料电池,通常用NaOH溶液做电解液,其正极反应为:O2+2H2O+4e-===4OH-
B.常温下,PH均为5的醋酸和硫酸铝两种溶液中,由水电离出的氢离子浓度均为1×10-9 mol・L-1
C.溴化钠溶液中加入少量新制氯水充分反应后,再加入少量苯振荡静置后上层颜色变浅,下层颜色变为橙红色
D.导电、缓慢氧化、品红褪色和久置浓硝酸变黄都一定属于化学变化
参考答案:A
本题解析:硫酸铝水解促进水的电离,则溶液中由水电离出的氢离子浓度均为1×10-5 mol/L,B不正确;苯的密度小于水的,则C中上层变为橙红色,C不正确;导电不一定是化学变化,例如金属导电,D不正确,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,在注重对学生基础性知识巩固和训练的同时,侧重对学生能力的培养和基础知识的巩固和训练。也有助于调动学生的学习兴趣和学习积极性,激发学生学习化学的热情。
本题难度:简单
2、填空题 某兴趣小组在课外活动中对某溶液进行了多次的检测,其中的三次检测结果如下表所示,请回答下列问题:
| 溶液中检测出的溶质
|
第一次
| KCl、K2SO4、Na2CO3、NaCl
|
第二次
| KCl、BaCl2、Na2CO3、NaCl
|
第三次
| KCl、K2CO3、Na2SO4、NaCl
|
(1)三次检测结果中,第 次的结果肯定不正确。
(2)在检测时,为了确定溶液中是否存在SO42-、CO32-和Cl-,该小组的学生进行了如下表所示的实验,请仔细分析实验,将表格补充完整:
实验步骤
| 实验操作
| 实验目的
| 反应的离子方程式
|
第一步
| 向溶液中滴加过量的硝酸
| 检验 ① 的存在
| ②
|
第二步
| 继续滴加过量的 ③ 溶液
| 检验SO42-的存在
| ④
|
第三步
| 过滤,再向滤液中滴加 ⑤ 溶液
| 检验 ⑥ 的存在
| Ag++Cl- = AgCl↓
|
(3)在上述实验的第一步中,能否将硝酸改为稀盐酸? (填“能”或“不能”,如果填“能”,则不用说理由;如果填“不能”,则说明理由)。
参考答案:(1)二
(2)① CO32- ② 2H+ + CO32- = CO2↑ + H2O
③ Ba(NO3)2溶液 ④ Ba2+ + SO42- = BaSO4↓ ⑤ AgNO3溶液⑥ Cl-
(3)不能 若加入盐酸,则引入Cl-
本题解析:(1)因BaCl2+Na2SO4=BaSO4↓+2NaCl;BaCl2+K2CO3=BaCO3↓+2KCl,所以氯化钡与硫酸钠在同一溶液中不共存,碳酸钾和氯化钡在同一溶液中不共存,三次检测中,第二次检测结果肯定不正确,故(2)用三种试剂将三种离子检验出来,每加一种试剂能够检验出一种离子,此时要注意每加入一种试剂只能与一种离子结合,检验氯离子可以使用银离子,检验硫酸根离子可以使用钡离子,检验碳酸根离子可以使用氢离子,而碳酸根离子和钡离子都可以与钡离子离子结合成沉淀,所以需先检验碳酸根离子,此时可以加入稀硝酸,其次检验硫酸根离子,离子反应方程式为2H+ + CO32- = CO2↑ + H2O,此时加过量的硝酸钡溶液,检验并除去硫酸根离子,离子反应方程式为:Ba2+ + SO42- = BaSO4↓,最后检验氯离子离子,可以加入硝酸银。(3) 不能加入盐酸,若加入盐酸,则引入Cl-。
考点:物质的检验和鉴别的实验方案设计;离子共存问题。
本题难度:困难
3、选择题 下列各组离子在指定溶液中能大量共存的是( )
①无色溶液中:K+、Cl-、NO-3、MnO4-?
②pH=11的溶液中:CO2-3、Na+、S2-、SO32-
③水电离的c(H+)=1×10-13mol/L的溶液中:Cl-、HCO-3、NH+4、S2O2-3
④加入Mg能放出H2的溶液中:Mg2+、NH+4、K+、Cl-
⑤酸性溶液中:Fe2+、NO-3、I-、Al3+.
A.①②
B.③⑤
C.②④
D.④⑤
参考答案:①因MnO4-在溶液中为紫色,与无色溶液不符,故①错误;
②pH=11的溶液显碱性,在碱性溶液中该组离子之间不反应,则能够共存,故②正确;
③水电离的c(H+)=1×10-13mol/L的溶液,水的电离受到抑制,溶液为酸或碱溶液,HCO3-既能与酸反应又能与碱反应,则一定不共存,故③错误;
④加入Mg能放出H2的溶液中显酸性,离子之间不反应,则能共存,故④正确;
⑤酸性条件下Fe2+、NO-3能发生氧化还原反应,NO-3、I-能发生氧化还原反应,则不能共存,故⑤错误;
故选C.
本题解析:
本题难度:简单
4、选择题 在指定环境中,下列各组离子一定可以大量共存的是(?)
A.使pH试纸呈红色的溶液: 、
、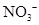 、
、 、
、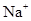
B.常温下,在 的溶液:
的溶液: 、
、 、
、 、
、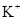
C.加入铝粉放出氢气的溶液: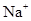 、
、 、
、 、
、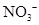
D.使无色酚酞试液显红色的溶液: 、
、 、
、 、
、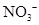
参考答案:B
本题解析:A中溶液显酸性,在酸性溶液中NO3-和Fe2+能发生氧化还原反应。B中溶液显酸性,能大量共存。加入铝粉放出氢气的溶液可能显酸性,也可能显碱性。显碱性,NH4+不能大量共存。显酸性,硝酸和铝反应不能生成氢气。D中溶液显碱性,NH4+不能大量共存。答案选B。
本题难度:一般
5、选择题 下列各组离子在指定溶液中,能大量共存的是
[? ]
A.溶解铝后得到的无色溶液:Na+、K+、Cl-、HCO3-
B.由水电离出的c(H+)=10-12mol/L的溶液中:Cl-、CO32-、NO3-、NH4+
C.加入Mg能放出H2的溶液中: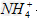 、Cl-、K+ 、SO42-
、Cl-、K+ 、SO42-
D.中性溶液中:Fe3+、Al3+、NO3-、Cl-
参考答案:C
本题解析:
本题难度:一般