��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ѧ�뼼����������ҽѧ�������������,����˵���д������
A��̫���ܵ�ذ��еĹ���Ԫ�����ڱ���λ�ڽ�����ǽ����Ľ���λ��
B������ͣ������װ�������ʩ���ɽ�����β����CO��NOx��Ӧ����������
C��������71���϶Ⱦ���ɱ������H1N1���в�������Ϊ�����ĵ��������ȷ�������
D����K2FeO4ȡ��Cl2��������ˮ����ɱ���������ã��Ҳ����γ��°������ˮ����
�ο��𰸣�D
���������
�𰸣�D
D.����ȷ����K2FeO4ȡ��Cl2��������ˮ������ɱ���������ã������γ��°�����о�ˮ���ã�4K2FeO4��H2O="4Fe" (OH)3��3O2��8OH�D ,���ɵ�����Fe (OH)3�γɽ��壬�������ԣ����Ծ�ˮ��
A�����ǰ뵼�壻B��4CO��2NO2 N2��4CO2��C����ȷ��
N2��4CO2��C����ȷ��
�����Ѷȣ�һ��
2������� ˮ��һ����Ҫ����Ȼ��Դ���������������治��ȱ�ٵ����ʡ�ˮ������ֱ��Ӱ�����彡��
��1�����н϶�______________��ˮ��ΪӲˮ��Ӳˮ���Ⱥ�������������ӷ���ʽΪ__________________________( д������һ�ֳ�����ļ���) ��
��2����ͼΪij����ˮ������Ȼˮ�Ʊ�����ˮ(ȥ����ˮ)�Ĺ�������ʾ��ͼ��

�ٻ���̿��������__________________��O3�������ŵ���________________��
��A��B�з��õ��������Ʒֱ��ǣ�A__________________��B_______________��A��B�з��õ������Ƿ���Ի���?��˵��ԭ��________________________________________��
��3��ͨ��ʩ��һ��ѹ��ʹˮ����ͨ����Ĥ��������ӻ����ӽ���, �Ӷ���ô���ˮ�ķ�����Ϊ??��������������ˮʱ, ʹ����ͨ����Ĥ���ƶ�����??��
��4����������ˮ�Ĵ���ʱ, ������еķ����Dzⶨˮ�� ?��
��5��ij �� �� �� ˮ ��c(Ca2+)Ϊ1.0��10-3mol/L, c(Mg2+)Ϊ5.0��10-4mol/L,c(HCO3_)Ϊ8.0��10-4mol/L������ҩ��������1000L ,Ӧ����Ca(OH) 2?g , Na2CO 3 __________ g ��
�ο��𰸣���1��C a2+�� M g2+ ?(2�֣�C a2++ 2 H C O3�� 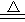 CaC O 3��+C O 2��+
CaC O 3��+C O 2��+
H 2O( ��?Mg2++ 2HCO3��  MgCO3��+CO2��+H2O? MgCO3+2H2O=Mg(OH)2+CO2��+H2O )(2�֣�
MgCO3��+CO2��+H2O? MgCO3+2H2O=Mg(OH)2+CO2��+H2O )(2�֣�
��2��������ˮ�е��л���(��ȥ��ˮ�е���ζ)��1�֣��ڷ�Ӧ�������������ӽ�����֬�������ӽ�����֬��2�֣�ˮ�е�Ca2+��Mg2+������������֬�е�OH- ����Mg(OH)2��Ca(OH)2������ɶ����������ӽ�����֬��1�֣�
��3�������� ��1�֣����Ʋ��糡����1�֣�
��4���絼�ʻ�����ʣ�1�֣���5)66.6 ��2�֣�? 116.6��2�֣�
�����������1������Ӳˮ�ĸ�����н϶�Ca2����Mg2����ˮ��Ӳˮ���ڼ��ȵ������£�̼�����ο��Էֽ�����̼���Σ�C a2++ 2 HCO3��  CaCO 3��+CO 2��+H 2O( ��Mg2++2HCO3��
CaCO 3��+CO 2��+H 2O( ��Mg2++2HCO3�� MgCO3��+CO2��+H2O ��MgCO3+2H2O=Mg(OH)2+CO2��+H2O )��
MgCO3��+CO2��+H2O ��MgCO3+2H2O=Mg(OH)2+CO2��+H2O )��
��2���ٻ���̿������Ϊ����ˮ�е��л����ȥ��ˮ�е���ζ����O3�������ŵ��Ƿ�Ӧ����������AΪ�����ӽ�����֬��BΪ�����ӽ�����֬��ˮ�е�Ca2+��Mg2+������������֬�е�OH- ����Mg(OH)2��Ca(OH)2������ɶ����������ӽ�����֬��
��3������������һ���������ӽ���Ĥ���к�ˮ�����ķ���������ӵ糡�������£�ˮ��Һ�����������ӻ�ֱ��������ƶ���������м����һ�ֽ���Ĥ���Ϳ��ܴﵽ����Ũ����Ŀ�ģ����Ե�����������ˮʱ��ʹ����ͨ����Ĥ���ƶ����ǵ��Ʋ��糡�����ʴ�Ϊ�������������Ʋ��糡������
��4����Ϊˮ�ĵ���̶ȼ�С�����Դ�ˮ�Ǽ���������ģ����Ҫ��������ˮ�Ĵ���ʱ��������еķ����Dzⶨˮ�ĵ絼�ʻ�����ʣ�
��5)c��Ca2����Ϊ1 .0��10-3mol��L��1��c��Mg2����Ϊ5.0��10-4mol��L��1��c��HCO3����Ϊ8.0��10-4mol��L��1������ҩ��������1000L��
n��Ca2����=1000L��1.0��10-3mol��L��1=1mol��n��Mg2����=1000L��5.0��10-4mol��L��1=0.5mol��n��HCO3����=1000L��8.0��10-4mol��L��1=0.8mol��
�����������Ʒ����ķ�ӦΪ��
Mg2��+2OH��=Mg(OH)2��?
0.5mol 1mol?
HCO3��+OH��=CO32��+H2O
0.8mol 0.8mol
����Ҫn��OH����=1.8mol��
����ҪCa(OH)2������Ϊ1.8mol��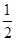 ��74g��mol��1=66.6g��
��74g��mol��1=66.6g��
ˮ��Һ��Ca2�����ʵ���Ϊ1mol+0.9mol=1.9mol��
������Ҫ�����̼�������Ϊ1.9mol-0.8mol=1.1mol��������Ϊ1.1mol��106g��mol��1=116.6g��
�ʴ�Ϊ��66.6��116.6��
�����Ѷȣ�һ��
3��ѡ���� ���н���ұ���ķ�Ӧԭ����������ǣ�?����
A��2NaCl�����ڣ�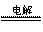 2Na��Cl2��
2Na��Cl2��
B��Al2O3��3H2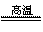 2Al��3H2O
2Al��3H2O
C��Fe3O4��4CO 3Fe��4CO2��
3Fe��4CO2��
D��2HgO 2Hg��O2��
2Hg��O2��
�ο��𰸣�B
���������������ұ��һ���Ǹ��ݽ���������ѡ������Խǿ�ģ����õ�ⷨ��Խ�����õĽ��������ȷֽⷨ�������м�Ľ���һ����û�ԭ����ԭ�����ǻ��õĽ�����Ӧ��ͨ����ⷨ����ҵ���õ�����ڵ���������ұ�������������Դ�ѡB��
�����Ѷȣ���
4��ѡ���� �����й�һЩ��ҵ����ԭ�ϵ������У�������ǣ�������
A������ͨ��������Ҫԭ���Ǵ��ʯ��ʯ��ʯӢ
B����ɫ����������ͨ�����м����������廯��������ͭ��С����
C����������½ṹ�մɿ��ɹ�͵����ڳ��·�Ӧ�Ƶ�
D��������ͨˮ�����Ҫԭ����ճ����ʯ��ʯ
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� �����뻯ѧ������أ����ж�Ӧ��ϵ����ȷ����
?
| ����
| ��Ҫ��ѧ�ɷ�
|
A��
| �մɲ;�
| ������
|
B��
| �����оƬ
| �����
|
C��
| �Ͻ��
| ��̼����ȺϽ�
|
D��
| ���ɰ
| ��������
�ο��𰸣�D
���������D ��Ӧ������ɰ��Ҫ��ѧ�ɷ���SiC
�����Ѷȣ�һ��
|