微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列过程合乎实际并用于工业生产的是(?)
A.钠在氯气中燃烧制氯化钠
B.氯化铵与氢氧化钙共热制氨气
C.浓盐酸与二氧化锰共热制氯气
D.氯气与石灰乳反应制漂白粉
参考答案:D
本题解析:略
本题难度:简单
2、填空题 (8分)【化学-化学与技术】
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g) 2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
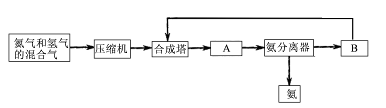
(1)合成氨所需要的原料气中,氮气取自?,氢气来源于?。
(2)对原料气进行净化处理的目的是?。
(3)设备A的名称是??,设备B的名称是??。
(4)在10~30Mpa时,工业合成氨选择400~500 ℃的温度进行反应,主要原因是?。
(5)据《科学》杂志报道,希腊化学家在常压下将氢气和用氢气稀释的氮气分另通入一个加热到570 ℃的电解池(如图)中,氢和氮在电极上合成了氨,且转化率达到了78%。
则阳极反应为?,阴极反应为?。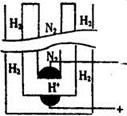
参考答案:⑴空气(1分)?水和碳氢化合物(1分)?⑵防止催化剂中毒(1分)
⑶冷凝器(1分)?循环压缩机(1分)
⑷温度500 ℃是因为温度太高,平衡混合物中氨的含量太低;温度太低,则化学反应速率太小。而且500 ℃,催化剂活性最大。(1分)
⑸H2-2e-=2H+(1分)? N2+6e-+6H+=2NH3(1分)
本题解析:⑴空气的主要成分是氮气,所以合成氨所需要的原料气中,氮气取自空气。而氢气来源于水和碳氢化合物。
⑵原料气中含有杂质,如果不处理会造成催化剂中毒,所以对原料气进行净化处理,是为了防止催化剂中毒。
⑶设备A为冷凝器,设备B为循环压缩机。
⑷选择400~500 ℃的温度,是综合反应速率、反应限度及催化剂活性等考虑。因为温度太高,平衡混合物中氨的含量太低;温度太低,则化学反应速率太小。而且500 ℃,催化剂活性最大。
⑸该装置为电解池,阳极失去电子,所以氢气在阳极通入,阳极反应为H2-2e-=2H+,阴极得到电子,因此氮气在阴极通入,所以阴极反应为N2+6e-+6H+=2NH3。
本题难度:一般
3、选择题 下列说法中,不正确的是
A.现代科学技术的发展和环境问题的解决离不开化学科学
B.门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路
C.绿色化学最显著的特征是在生产化工产品过程中必须利用绿色植物为原料
D.植物的光合作用是地球上规模最大的化学反应,在生物体内把光能转变为化学能
参考答案:C
本题解析:现代科学技术的发展和环境问题的解决离不开化学科学,A正确;门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路,B正确;“绿色化学”的核心是利用化学原理从源头上减少和消除工业生产对环境的污染;反应物的原子全部转化为期望的最终产物,而并不是必须利用绿色植物为原料,选项C不正确;植物的光合作用是地球上规模最大的化学反应,在生物体内把光能转变为化学能,D正确,答案选C。
点评:该题是常识性知识的考查,难度不大。注意相关知识的积累和总结即可,有利于培养学生的学习兴趣,调动学生的学习积极性。
本题难度:简单
4、填空题 A为无色晶体,B为淡黄色固体;X、C、E、G均为气体。其相关关系如图1-12所示:
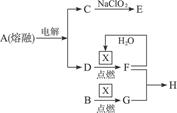
图1-12
(1)晶体A常用作城市道路融雪剂,由此可知C为__________,D为__________;
(2)E是新型饮用水消毒剂,其分子构型与G相同,由C生成E的化学方程式是____________________。E作为饮用水消毒剂的主要优点是:①____________________,②____________________。
(3)F与G生成H的化学方程式是____________________。
参考答案:(1)Cl2? Na?(2)2NaClO2+Cl2====2ClO2↑+2NaCl?①ClO2消毒效率是同质量Cl2的2.63倍?②ClO2不会与水中的有机物反应生成氯代烃?(3)Na2O2+SO2====Na2SO4
本题解析:“晶体A常用作城市道路融雪剂”是本题的题眼――A是氯化钠;电解熔融的氯化钠可得钠和氯气;氯气与NaClO2得到的气体消毒剂应是二氧化氯;钠在氧气中点燃可得过氧化钠;硫在空气中点燃则得到二氧化硫;二氧化硫与过氧化钠反应生成的是硫酸钠。
本题难度:简单
5、选择题 ①国际互联网上报道:“目前世界上有近20亿人患有缺铁性贫血”。我国政府现已启动“酱油补铁工程”。这里的铁指的是
A.铁元素
B.铁单质
C.四氧化三铁
D.硫酸铁
参考答案:A
本题解析:考查化学与生活、生产等。这里的铁应该是铁元素,答案选A。
本题难度:简单