微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于可逆反应:N2(g)+3H2(g) 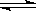 2NH3(g)正反应为放热反应,下列各组条件变化时,两项均能使平衡向右移动的是
2NH3(g)正反应为放热反应,下列各组条件变化时,两项均能使平衡向右移动的是
A.加压、升温
B.加压、降温
C.减压、升温
D.减压、降温
参考答案:B
本题解析:A错,加压平衡右移,但升温,由于正反应为放热反应,平衡将向左移动;B正确;C错,减压平衡左移,升温平衡左移;D错,减压平衡左移,降温平衡右移;
本题难度:简单
2、填空题 (1)下列各物质中①0.5mol氨气;②标准状况下33.6L氦气;③18.0g水,所含原子个数由大到小的顺序为______.
(2)常温常压下,同体积的CO、CO2分子个数比______,氧原子个数比______,质量之比______,电子数之比______.
参考答案:(1)0.5mol氨气含有的原子数=0.5mol×NA×4=2NA,标准状况下33.6L氦气含有的原子数=33.6L22.4L/molNA×1=1.5NA,
18.0g水含有的原子数=18g18g/molNA×3=3NA,所以所含原子个数由大到小的顺序为③①②,
故答案为:③①②;
(2)同温同压下,同体积的气体所含分子数相等,且其物质的量相等,所以同体积的CO、CO2分子个数比1:1,一个一氧化碳分子中含有1个氧原子,一个二氧化碳分子中含有2个氧原子,所以氧原子个数之比是1:2,一氧化碳的摩尔质量是28g/mol,二氧化碳的摩尔质量是44g/mol,所以一氧化碳和二氧化碳的质量之比是28:44=7:11,一个一氧化碳分子中14,二氧化碳分子中含有22,所以含有电子数之比是14:22=7:11;
故答案为:1:1;1:2;7:11;7:11.
本题解析:
本题难度:一般
3、选择题 设NA代表阿伏加德罗常数,下列说法正确的是(?)
A.24g金属镁变为镁离子时失去的电子数为NA
B.18g水所含的电子数目为NA
C.标准状况下,11.2L SO3所含的分子数目为0.5NA
D.在常温常压下32g氧气所含的原子数目为2NA
参考答案:D
本题解析:一个镁原子变为镁离子时失去2个电子,24g金属镁的物质的量为24/24=1mol,1mol金属镁变为镁离子是失去电子为2mol,数目为2NA,A错误;18g水的物质的量为18/18=1mol,一个水分子中含有的电子数目为10,所以18g水中含有的电子数目为10 NA,B错误;标准状况下,SO3为固体,已知体积无法进行计算,C错误;32g氧气的物质的量为32/32=1mol,一个氧气中含有2个氧原子,所以1mol氧气中含有氧原子数目为2NA。D正确。
本题难度:简单
4、选择题 设NA为阿佛加德罗常数,下列叙述正确的 (? )
A.1molCl2与足量Fe反应,转移的电子数为3
B.标准状况下,22.4LNO和HCl混合气体所含分子数为2NA
C.标准状况下,11.2L三氧化硫中所含的氧原子数等于1.5NA
D.配制含0.5NA H+的硫酸溶液需密度为1.84g・cm-3的98%浓硫酸约13.6mL
参考答案:D
本题解析:A 错误,1molCl2与足量Fe反应,转移的电子数为2mol
B 错误,标准状况下,22.4LNO和HCl混合气体所含分子数为NA
C 错误,标准状况下,三氧化硫是固体
D 正确,根据浓硫酸稀释前后溶质的物质的量不变计算。
本题难度:一般
5、选择题 NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.常温常压下,22.4L的D2、H2组成的气体分子数为NA
B.pH=1的甲酸溶液中,HCOO-和OH-数目之和为0.1NA
C.SiO2晶体中,有NA个Si就有2NA个Si―O键
D.9.6g铜与足量的稀硝酸反应,生成NO分子数一定为0.1NA
参考答案:D
本题解析:常温常压下的Vm>22.4L/mol,故22.4L的D2、H2组成的气体小于1mol,故A错;未告诉溶液的体积,无法计算HCOO-和OH-的数目,故B错;SiO2晶体中,有NA个Si就有4NA个Si―O键,因为每个硅原子与4个O相结合,故C错;3Cu~2NO,故生成0.1 mol NO。所以选D。
本题难度:简单