微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的转化率不高。
(1)已知:1 mol N2(g)与适量H2(g)完全反应,生成NH3(g),放出92.2 kJ热量,写出反应的热化学方程式:____________________。
(2)若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1______K2 (填“>” “=” 或 “<” )。
(3)在一定温度下,向容积不变(始终为10L)的密闭容器中加入2 mol N2、8 mol H2及固体催化剂。
10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,此时氨气的体积分数为______,用氮气表示的反应速率为:____________。若想提高氨气的产率,根据化学平衡移动原理,请提出合理的建议:__________________(任意写一条)。
(4)在上述相同条件下,若起始时加入4 mol NH3、2 mol H2及固体催化剂,反应达到平衡时NH3的体积分数比(3)中______(填“大”、“小”或“相等”)。
(5)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。
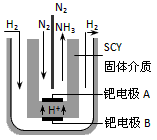
请回答:在电解法合成氨的电解池中______(填“能”或“不能”) 用水作电解质溶液的溶剂,原因是__________________。钯电极A是电解池的______极(填“阳”或“阴”),该极上的电极反应式是__________________。
2、选择题 把物质的量均为0.1mol的AlCl3、CuCl2和H2SO4溶于水制成100ml的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同。则下列描述正确的是:
[? ]
A.电路中共转移0.9mol电子
B.阳极得到的气体中有O2,且其物质的量为0.35mol
C.阴极质量增加3.2g
D.铝元素以Al(OH)3的形式存在
3、选择题 在下列说法正确的是( )
A.镁、铝和NaOH溶液所形成的原电池中,镁作正极
B.用电解法精炼粗铜时,粗铜作阴极
C.电镀时,镀件作阳极,含有镀层金属阳离子的溶液作电镀液
D.电解质溶液的导电过程就是该溶液的电解过程
4、选择题 某电解池内盛有CuSO4溶液,插入两根电极,接通直流电源后,欲达到如下要求:①阳极质量不变?②阴极质量增加?③电解液pH减小,则应选用的电极是(? )
A.阴、阳两极都用石墨棒
B.铜棒作阳极,铁棒作阴极
C.铁棒作阳极,铜棒作阴极
D.铜棒作阳极,铜棒作阴极
5、选择题 下图所示装置中,X是铁,Y是石墨电极,a是硫酸钠溶液,实验开始前,在U 形管的两边同时各滴入几滴酚酞试液,下列叙述正确的是
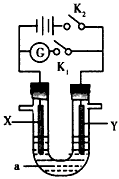
[? ]
A.合上K1,断开K2,X极放出H2
B.合上K1,断开K2,Y极为阳极
C.合上K2,断开K1,Y极的电极反应式为:O2+2H2O+4e-=4OH-
D.合上K2,断开K1,电解一段时间,X电极附近溶液呈红色