��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���ڡ�����Ȼ�ͭ��Һ��pH�仯�����⣬��ѧ�������ֲ�ͬ�Ĺ۵㣺
�۵�һ���������ɡ���Ϊ����Ȼ�ͭ��Һ����Һ��pH���ߡ�
�۵������ʵ���ɡ�������������Ρ���ȷ��ʵ��ⶨ��֤������Ȼ�ͭ��ҺʱpH�ı仯��ͼ��ʾ���߹�ϵ��
��ش��������⣺

(1)���ǰ�Ȼ�ͭ��Һ��pH����A��λ�õ�ԭ���ǣ��������ӷ���ʽ˵����______________________
(2)�������ɡ����ֹ۵�����������ǣ�____________________��
(3)��ʵ���ɡ��Ľ����ǣ�____________________��������������ȷ��ʵ�顱��ͨ��__________ȷ���ġ�
(4)��ֺ��ֹ۵㣬�����ֹ۵�������ǣ�___________________________ ���ӻ�ѧԭ������˵������
�ο��𰸣�(1)Cu2++2H2O Cu(OH)2+2H+
Cu(OH)2+2H+
(2)���ʱ������CuCl2���٣���ҺŨ�ȼ��٣�����pH����
(3)pH�Ƚ��ͣ�Ȼ�������ȶ���pH
(4)��ʵ���ɡ��۵���ȷ����������Cl2����ˮ����ˮ��Ӧ���������ᣬ��ʹpH���ͣ�Cl2���ͺ�pH���ٱ仯
���������
�����Ѷȣ�һ��
2��ѡ���� ��ʢ��ˮ�ĵ����м��뺬�����ʵ�����Ag+��Pb2+��K+��SO42-��NO3-��Br������-����ֽ��裬Ȼ���ö��Ե缫��⣬ͨ��Ƭ�̺���������ͻ�ԭ��������ʵ���֮��Ϊ
A��1��2
B��8��1
C�� 1��1
D��80��108
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
3�������� ��ͼ��װ�ý��е��ʵ�飺A����ͭп�Ͻ�B��Ϊ��ͭ��������к���������ͭ���ӡ�ͨ��һ��ʱ�����A��ǡ��ȫ���ܽ⣬��ʱB����������7.68g����Һ��������0.03g����A�Ͻ���Cu��Znԭ�Ӹ�����Ϊ
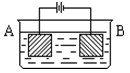
A��3�U1
B��4�U1
C��2�U1
D�������
�ο��𰸣�A
���������B����������7.68g����Һ��������0.03g�����ԺϽ��������7.71g����Ӧ��ת�Ƶ���Ϊ ����Ͻ���Cu��Zn�����ʵ����ֱ�Ϊx��y����64x��65y��7.71��2x��2y��0.24�����x��0.09mol��y��0.03mol������Cu��Znԭ�Ӹ�����Ϊ3�U1��
����Ͻ���Cu��Zn�����ʵ����ֱ�Ϊx��y����64x��65y��7.71��2x��2y��0.24�����x��0.09mol��y��0.03mol������Cu��Znԭ�Ӹ�����Ϊ3�U1��
�����Ѷȣ���
4��ѡ���� ����ʵ�����������ͽ��۾���ȷ����
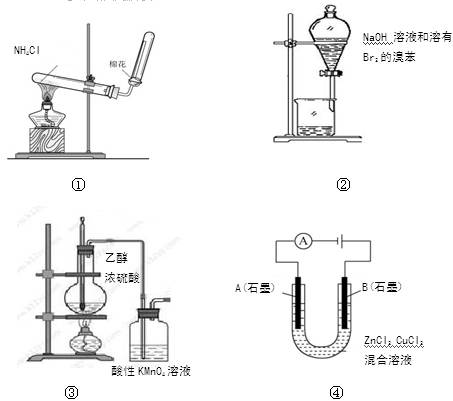
ѡ��
| ����
| ����
| ����
|
A
| �ٽ�ʪ��ĺ�ɫʯ����ֽ�����Թܿ�
| ��ֽ����ɫ
| NH4Cl���Ȳ��ֽ�
|
B
| ��������
| �²�Һ����ɫ��dz
| NaOH��Һ�ɳ�ȥ�����屽�е�Br2
|
C
| �ۼ���
| ϴ��ƿ����Һ��ɫ
| ��������ϩ
|
D
| ��ͨ��
| A�����к�ɫ��������
| п�Ľ����Ա�ͭǿ
|
�ο��𰸣�BD
���������A���Ȼ�粒������ȷֽ����ɰ������Ȼ��⣬�������Թܿ������ַ�Ӧ�����Ȼ�泥���ʪ���ɫʯ����ֽ����ɫ������B����������������Һ��Ӧ����������ˮ���廯�ƺʹ������ƣ��ɸ�װ�ó�ȥ�屽�е��壬��ȷ��C��������ƿ���Ҵ��ӷ����Ҵ�Ҳ��ʹ���Ը��������Һ��ɫ������֤����������ϩ������D��ͨ���A�缫���к�ɫ����������˵�������ԣ�Cu2����Zn2����֤��п�Ľ����Ա�ͭǿ����ȷ��
���㣺���黯ѧʵ�鷽���ķ��������ۡ�
�����Ѷȣ�һ��
5��ѡ���� ���й��ڵ���˵����ȷ����
A������ǰѻ�ѧ��ת��ɵ���
B�����ص���������������Ӧ������������ԭ��Ӧ
C�����ʱ��Һ�п����ӵ���
D����ҵ��ͨ���������MgO�Ʊ�Mg����
�ο��𰸣�B
�������������ǰѵ���ת��Ϊ��ѧ�ܵ�װ�ã�A����ȷ�����ص�����ʧȥ���ӷ���������Ӧ�������õ����ӷ�����ԭ��Ӧ��A��ȷ�����ʱ��Һ�п����ӵĶ����ƶ����磬C����ȷ����ҵ��ͨ����������Ȼ�þ�Ʊ�Mg���ʣ�D����ȷ����ѡB��
�����������Ǹ߿��еij������㣬�����е��Ѷȵ����⡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ�����ѵ��������������ѧ��������û���֪ʶ���ʵ����������������⿼���֪ʶ��Ƚ϶࣬���ܻ������ѶȲ���ס���ɡ�
�����Ѷȣ���