微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是?①氯气的性质很活泼,它与氢气混合后立即发生爆炸?②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收?③新制氯水的氧化性强于久置氯水④检验HCl气体中是否混有Cl2方法是将气体通入硝酸银溶液?⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水
A.①②③
B.②③④
C.③
D.③⑤
参考答案:B
本题解析:略
本题难度:简单
2、选择题 已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下列描述正确的是? ( )?
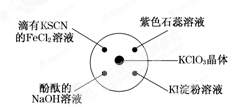 ?
?
A.淀粉KI溶液中变蓝,说明Cl2具有氧化性
B.滴有酚酞的NaOH溶液褪色,说明Cl2具有酸性
C.石蕊溶液先变红后褪色,说明Cl2具有漂白性
D.滴有KSCN的FeCl2溶液变红,说明Cl2具有还原性
参考答案:A
本题解析:考查氯气的性质
A.正确
B.由于氯气在溶液中生成具有漂白性的次氯酸,使酚酞褪色,排除
C.石蕊溶液先变红说明生成了酸性物质,后褪色说明生成了具有漂白性的次氯酸,排除
D.氯气将FeCl2氧化为FeCl2,与KSCN形成血红色的络合物,不正确
答案为A
本题难度:一般
3、实验题 实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是?(写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是?(写编号),写出微热时的反应方程式??;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
2KCl + 2MnCl2 + 5Cl2 ↑?+ 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中?元素被氧化,?是氧化剂。当有1mol电子转移时,可生成气体?升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:
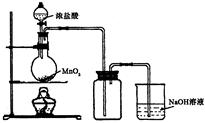
写出圆底烧瓶中发生反应的化学方程式_??
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.
参考答案:(1) A?(2) C ; NaCl + H2SO4 NaHSO4? +? HCl↑;(3)(a)?
NaHSO4? +? HCl↑;(3)(a)?
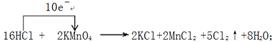 ? Cl元素;KMnO4;11.2
? Cl元素;KMnO4;11.2
(b) ①? MnO2 + 4HCl(浓)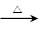 2MnCl2 + Cl2↑ + 2 H2O?
2MnCl2 + Cl2↑ + 2 H2O?
②NaOH;? Cl2 ?+ 2 OH- Cl-?+?ClO- +? H2O
Cl-?+?ClO- +? H2O
本题解析:根据装置图可知,A适用于固体和固体加热制备气体的。B装置适用于液体和固体或液体和液体之间不需要加热制备气体的。C装置适用于液体和固体或液体和液体之间需要加热制备气体的。
(1)实验室用氯酸钾和二氧化锰制氧气时,属于固体和固体之间加热制备气体的,所以可选用的发生装置是A。
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,属于液体和固体之间加热制备气体的,所以可选用的发生装置是C,反应的化学方程式是NaCl + H2SO4 NaHSO4 + HCl↑。
NaHSO4 + HCl↑。
(3)(a)根据方程式可知,Mn元素的化合价从+7价降低到+2价,得到5个电子,则高锰酸钾是氧化剂。氯化氢中氯元素的化合价从-1价升高到0价,失去1个电子,则氯化氢是还原剂,氯元素被氧化。所以根据电子得失守恒可知,其表示方法是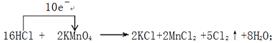
当有1mol电子转移时,可生成0.5mol氯气,在标准状况下的体积是22.4L/mol×0.5mol=11.2L。
(b)① 在加热的条件下,二氧化锰能把浓盐酸氧化生成氯气,则反应的化学方程式是 MnO2 + 4HCl(浓)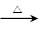 2MnCl2 + Cl2↑ + 2 H2O。
2MnCl2 + Cl2↑ + 2 H2O。
②氯气有毒,需要尾气处理,试剂选用氢氧化钠溶液,反应的离子方程式是 Cl2 + 2 OH- Cl-?+?ClO- +? H2O。
Cl-?+?ClO- +? H2O。
点评:该题是高考中的常见题型,属于中等难度实验题的考查,该题紧扣教材基础知识,有利于调动学生的学习兴趣,激发学生的学习积极性,有利于培养学生规范严谨的实验设计能力,提升学生的学科素养。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
4、选择题 为防止吸入Cl2而引起中毒,可用浸透某种物质溶液的毛巾捂住口鼻,这种物质可能是?(?)
A.Na2CO3
B.KI
C.NaOH
D.浓氨水
参考答案:A
本题解析:Na2CO3+2Cl2+H2O=2NaCl+2HClO+CO2↑,NaOH溶液也可与Cl2反应生成无毒的NaCl和NaClO,但其碱性太强,对人有腐蚀作用;KI可以与Cl2反应生成I2,仍然有毒性;浓氨水对人也有强烈的刺激性和腐蚀性。
本题难度:简单
5、选择题 碘(ICl)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,能与许多非金属单质反应生成相应卤化物,能与水反应等。其与水反应的方程式为ICl+H2O HCl+HIO。 下列关于ICl的叙述中不正确的是(?)
HCl+HIO。 下列关于ICl的叙述中不正确的是(?)
A.ICl是一种有色物质
B.在许多反应中ICl是强氧化剂
C.在ICl与水的反应中,它既是氧化剂又是还原剂
D.与NaOH溶液反应生成的产物中有NaIO和NaCl
参考答案:C
本题解析:A、碘(ICl)的化学性质与卤素单质相似,而卤素单质都是有颜色,因此ICl也是一种有色物质。
B、ICl中碘元素的化合价为+1价,可降低为0价,具有强氧化性,可做氧化剂。
C、ICl+H2O HCl+HIO中没有元素的化合价发生变化,故该反应不是氧化还原反应,此叙述不正确。
HCl+HIO中没有元素的化合价发生变化,故该反应不是氧化还原反应,此叙述不正确。
D、由反应ICl+H2O HCl+HIO可看出,与NaOH反应后的产物应为NaIO和NaCl,正确。故答案为C。
HCl+HIO可看出,与NaOH反应后的产物应为NaIO和NaCl,正确。故答案为C。
点评:本题考查氧化还原反应,属于基础题,也是高考的常见考点。考生在复习备考中,应牢牢把握住基本概念,只有掌握了基本概念,才能很好的解答此类基础题型。
本题难度:简单