| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《常见的化学电源》考点巩固(2017年最新版)(八)
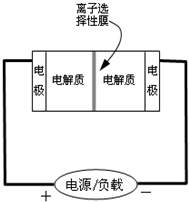 参考答案:①、有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,故①正确; 本题解析: 本题难度:一般 2、选择题 我国首创以铝―空气―海水电池作为能源的新型的海水标志灯,以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流,只要把灯放入海水数分钟,就会发出耀眼的白光。则电源的负极材料是?,负极反应为?;正极材料是?,正极反应为?。 参考答案:铝为负极,电极反应式为4Al → 4Al3++12e-,正极为石墨等惰性电极,反应为3O2+6H2O+12e-→ 12OH-。 本题解析:由铝―空气―海水电池靠空气中的氧气使铝不断氧化而产生电流可知,铝为负极,电极反应式为4Al → 4Al3++12e-,正极为石墨等惰性电极,反应为3O2+6H2O+12e-→ 12OH-。 本题难度:简单 3、填空题 (9分)右图是一个化学过程的示意图。已知甲池的总反应式为: 参考答案: 本题解析: 本题难度:简单 4、填空题 据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH- (1)放电时电极反应方程式:正极______;负极______. (2)充电时电解质溶液的pH逐渐______(填增大、减小),充电时每生成1molCH3OH转移______?mol电子. 参考答案:(1)放电时,相当于原电池的工作原理,正极是氧气发生得电子的还原反应,即O2+2H2O=4OH-+4e-,负极是甲醇发生失电子的氧化反应,即CH3OH+8OH-=6H2O+CO32-+6e-,故答案为:O2+2H2O=4OH-+4e-;CH3OH+8OH-=6H2O+CO32-+6e-; 本题解析: 本题难度:简单 5、选择题 铅蓄电池是广泛应用于汽车、柴油机车等的启动电源。产生电能时的电极反应分别为: 参考答案: 本题解析: 本题难度:困难 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《有关氧化还.. | |