��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڷ�Ӧ2SO2(g)+O2(g)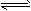 2SO3(g)����������Ӧ���ʵĴ�ʩ��
2SO3(g)����������Ӧ���ʵĴ�ʩ��
[? ]
A��ͨ�����O2
B�����������ݻ�
C����ȥ����SO3
D��������ϵ�¶�
2��ѡ���� ��Ӧ2X(g)��Y(g)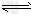 2Z(g)?����H<0���ڲ�ͬ�¶ȣ�T1��T2���£�����Z�����ʵ���n�뷴Ӧʱ��t�Ĺ�ϵ��ͼ��ʾ���������ж�����ȷ����
2Z(g)?����H<0���ڲ�ͬ�¶ȣ�T1��T2���£�����Z�����ʵ���n�뷴Ӧʱ��t�Ĺ�ϵ��ͼ��ʾ���������ж�����ȷ����
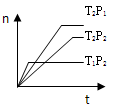
[? ]
A��T1��T2��P1��P2������ ?
B��T1��T2��P1��P2���� ?
C��T1��T2��P1��P2����? ?
D��T1��T2��P1��P2
3������� Ϊ���ٺ�����CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о����״���һ�ֿ�����ȼ�ϣ����ķе�Ϊ64.7�档�п�ѧ�������ɫ���룺�Ѻ���CO2�Ŀ�����ҵβ��ͨ��̼�����Һ�У�Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��õ��״����乹���������£�(���ԭ��������C-12?O-16?Ca-40?Ba-137)

�Իش��������⣺
��1��д���ֽ���з�����Ӧ�Ļ�ѧ����ʽ_________________________��?
��2����2��105Pa��300��ϳ����У�����CO2��H2��Ӧ����32g�״���ˮ���ų�49.5kJ����������д���ϳ����з�����Ӧ���Ȼ�ѧ����ʽ�� ______________________��?
��3���ںϳ����з������Ƿ��ȷ�Ӧ�����²����ڼ״������ɣ��ϳ�����ά��300��Ľϸ��¶ȵ�ԭ�������_______________����Ҫ��״��IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��(д2��)��________________?��______________��
��4���״���һ����Ҫ��������ȼ�ϵ�أ�����KOH���������Һ�������ĵ缫��ӦʽΪ��_____________________��
��5�����³�ѹ�£�����CO2ˮ��Һ�ĵ�pH=5.6��c?(H2CO3)=?1.5��10�C5mol/L��������ˮ�ĵ����H2CO3�Ķ������룬��H2CO3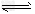 HCO3�C+?H+��ƽ�ⳣ��K=?_________?(����������2λ��Ч���֣���֪10�C5.6=2.5��10�C6)��?
HCO3�C+?H+��ƽ�ⳣ��K=?_________?(����������2λ��Ч���֣���֪10�C5.6=2.5��10�C6)��?
��6��ijͬѧ���ó������ⶨ������CO2����������������CaCO3��BaCO3���ܶȻ������ֱ�Ϊ4.96��10�C9��2.58��10�C9����ͬѧӦ��ѡ�ýϺ��ʵ��Լ���_________(����ĸ)��
A��Ba(OH)2��Һ?
B��Ca(OH)2��Һ?
C��BaCl2��NaOH�����Һ?
D��CaCl2��Һ?
4������� ˮú������Ҫȼ�Ϻͻ���ԭ�ϣ�����ˮ����ͨ�����ȵ�̿���Ƶã�
C(s)+H2O(g)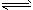 CO(g)+H2(g) ��H�� +131��3kJ��mol-1
CO(g)+H2(g) ��H�� +131��3kJ��mol-1
��1��������Ӧ�ﵽƽ�����ϵ�е�C(s)ȫ�����ߣ�ƽ��_______________�������� / ������ / ���ƶ�����
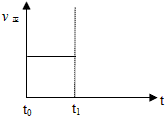
��2��������Ӧ��t0ʱ�̴ﵽƽ�⣨����ͼ��������t1ʱ�̸ı�ijһ������������ͼ�м�������t1ʱ��֮������Ӧ���ʣ���������ʱ��ı仯��
�� ��С�����������ʵ�߱�ʾ��
�� �����¶ȣ������߱�ʾ��
��3����֪ƽ��ʱT��ͬ��c(CO)��c(H2)��c(H2O)��ֵ��ȡ�һ���¶��£����������о�������������Ӧ����������̿�������������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д������Ӧ�Ŀո�

��4����֪��
2C(s) + O2(g) �� 2CO(g) ��H �� ��221��0 kJ��mo1-1
2CO(g) + O2(g) �� 2CO2(g) ��H �� ��566��0 kJ��mo1-1
2H2(g) + O2(g) �� 2H2O(g) ��H �� ��483��6 kJ��mo1-1
����24g̿��ȫת��Ϊˮú����Ȼ���ٳ��ȼ�գ��������̵��ʱ�Ϊ_____________kJ��
5������� ij�������ڹ�ũҵ������������������Ҫ���á���ش��������⣺
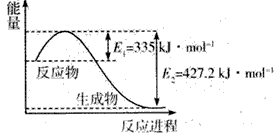
(1)��ͼ��N2��H2��Ӧ����2 mol NH3�Ĺ����������仯ʾ��ͼ��ÿ����1 mol NH3�ų�������Ϊ ______��
(2)�����Ϊ2L���ܱ������У����з�Ӧ��N2 (g) +3H2(g) 2NH3(g) ��H <0�����������ݣ�
2NH3(g) ��H <0�����������ݣ�
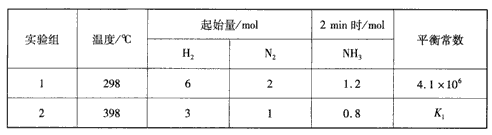
��ش��������⣺
����ʵ��1��2�ɵ�K1____ 4.1��106���>������=����<������
��ʵ��l����v(H2)��ʾ�ķ�Ӧ����Ϊ___��
�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�����ݵ���___������ţ���
A��������N2��H2��NH3�����ʵ���Ũ��֮��Ϊ1:3:2
B��v(N2)��=3v(H2)��
C��������ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
(3)��һ�������ºϳɰ���Ӧ�ﵽƽ����ں��������³��뺤��������Ӧ����___�����������С���� �䡱�����ں�ѹ�����³��뺤����ƽ��___�ƶ��������������������
(4) NH4Cl��Һ������������NH4+ˮ���Ե�ʡ���NH4 Cl����ˮ(D2O)��ˮ������ӷ���ʽΪ____ ��