微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列表述正确的是
[? ]
A.氯气溶于水的离子方程式是Cl2+H2O=2H++Cl-+ClO-
B.含有大量NO3-的溶液中,可以同时大量存在H+、Fe2+、Cl-、SO42-
C.常温下在AgNO3溶液中滴加NaCl溶液至不再有白色沉淀生成,再滴加KI溶液,沉淀由白色变黄色,证明常温下AgCl溶解度大于AgI溶解度
D.若NA表示阿伏加德罗常数的值,1mol C20H42的分子中含有的共价键数目为62 NA
参考答案:C
本题解析:
本题难度:一般
2、填空题 (14分)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
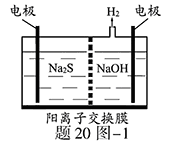
(1)将烧碱吸收H2S后的溶液加入到如题20图―1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2-―2e- S?(n―1)S+?S2-
S?(n―1)S+?S2- ?Sn2-
?Sn2-
①写出电解时阴极的电极反应式:?。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成?。
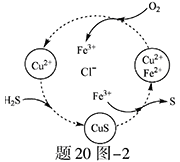
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如题20图―2所示。
①在图示的转化中,化合价不变的元素是?。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为?。
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有?。
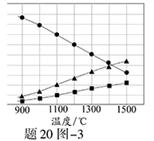
(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题20图―3所示,H2S在高温下分解反应的化学方程式为?。
参考答案:
(1)①? 2H2O+2e-=H2↑+2OH-
② Sn2-+2H+="(n-1)S↓+" H2 S↑
(2)①Cu、Cl?②0.5mol?③提高空气的比例(增加氧气的通入量)
(3)2H2S 2H2+S2
2H2+S2
本题解析:(1)阴极是水产生的氢离子放电;电解后生成Sn2-,与酸发生歧化反应反应生成硫单质和硫化氢;(2)根据电子守恒,硫化氢电子给了氧气,氧气得电子为0.5mol;增加铁离子含量,使硫化铜被充分氧化,所以需增加氧气使亚铁离子被充分氧化;(3)由图判断生成两种气体体积比为2:1,只能产生S2才符合题意。
本题难度:一般
3、选择题 下列各组离子在给定条件下一定能够大量共存的是(?)
A.使pH试纸呈红色的溶液中:Fe2+、ClO-、SO42-、Na+
B.c(H+)=1.0×10-13 mol/L 的溶液中:Na+、SO42-、Al O2-、CO32-
C.加入铝粉后能产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42-
D.由水电离出c(H+)=10-12 mol・L-1的溶液:K+、Al3+、Cl-、SO42-
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列各组离子一定可以大量共存的是( )
A.在含大量Al3+的溶液中:NH
、Na+、HCO3-、SO42-
B.能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3-
C.在水电离出的c(H+)=10-13mol?L-1?的溶液中:NH、[Al(OH)4]-、SO、NO
D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3-
参考答案:A.HCO3-与Al3+发生互促水解反应而不能大量共存,故A错误;
B.使甲基橙试液变红的溶液呈酸性,酸性条件下,离子之间不发生任何反应,可大量共存,故B正确;
C.水电离出的c(H+)=10-13mol?L-1 的溶液可能呈酸性,也可能成碱性,酸性条件下[Al(OH)4]-不能大量共存,碱性条件下NH4+不能大量共存,且二者之间发生互促水解反应,故C错误;
D.pH=1的溶液呈酸性,酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故D错误.
故选B.
本题解析:
本题难度:一般
5、选择题 下列各组离子能在溶液中大量共存,且溶液呈无色透明的是
[? ]
A.AlO2-?、CO32-?、Na+、K+?
B.Al3+、Cl-、MnO4-?、Na+
C.Na+、OH-、HCO3-、NO3-?
D.Fe2+、K+、H+、NO3-?
参考答案:A
本题解析:
本题难度:一般