微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,含有氯离子的是
A.氯化氢
B.食盐
C.氯酸钾
D.液氯
参考答案:B
本题解析:A错,只有HCL分子;B正确,食盐为离子化合物无分子含有氯离子;C错,氯酸钾中有钾离子和氯酸根离子;D错,只有氯分子;
本题难度:简单
2、填空题 二十一世纪世界资源争夺的重点是海洋。海底有石油、可燃冰、石油气、矿砂、锰结核的资源,海水中除有渔业资源外,还有食盐、溴、碘等许多化学资源,所有资源中最丰富的是水资源。
(1)海水中质量分数最高的元素是氧,该元素的原子核外电子占据的轨道共有________个能级,有________个未成对电子。
(2)水的沸点为100℃,氟化氢的沸点为19.5℃,水与氟化氢比较,稳定性较强的是_ _______。水的沸点比硫化氢高,其原因是___________________。
_______。水的沸点比硫化氢高,其原因是___________________。
(3)提取碘是将海带灼烧成灰,溶于水过滤,滤液中通入氯气,反应的离子方程式为_______________________________,再用四氯化碳将生成的单质碘______(填写实验操作名称)出来,最后用_________(填写实验操作名称)使碘和四氯化碳分离。
(4)海洋元素中的氯、溴、碘统称为海水中的卤素资源,它们的最外层电子排布都可表示为_____________________。
参考答案:(本题共24分)
(1)3?,? 2?。
(2)HF?。?水分子之间存在氢键?。
(3)2I-+Cl2 I2+2Cl-?,?萃取?,?蒸馏?。
I2+2Cl-?,?萃取?,?蒸馏?。
(4)ns2np5?。(每空各1分)
本题解析:略
本题难度:一般
3、选择题 下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
己知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O
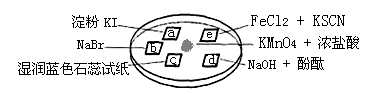
对实验现象的“解释或结论”正确的是
选项
| 实验现象
| 解释或结论
|
A
| a处变蓝,b处变红棕色
| 氧化性:Cl2>Br2>I2
|
B
| c处先变红,后褪色
| 氯气与水生成了酸性物质
|
C
| d处立即褪色
| 氯气与水生成了漂白性物质
|
D
| e处变红色
| 氧化性:Cl2 > Fe3+
|
?
参考答案:D
本题解析:KMnO4与浓盐酸发生反应产生氯气,A.在a处发生反应:Cl2+2KI=2KCl+I2. I2遇淀粉会变为蓝色。在b处发生反应:Cl2+2NaBr=2NaCl+Br2。这只能证明氧化性Cl2>Br2;Cl2> I2。但是不能证明Br2>I2。错误。B. 在c处发生反应Cl2+H2O HCl+HClO,HCl是酸,电离产生H+使溶液显酸性,能使湿润的蓝色石蕊试纸变红,由于还产生了有强氧化性的HClO,它能把有色物质氧化为无色物质,所以后来又褪色。错误。C.在d处发生反应:Cl2+2NaOH=NaCl+NaClO+H2O。由于碱被消耗,溶液的碱性减弱,所以酚酞的红色逐渐变浅。错误。D.在e处发生反应:2Fe2++Cl2= 2Cl-+2Fe3+;Fe3++ 3SCN-=Fe(SCN)3.溶液变为血红色。证明了氧化性Cl2 > Fe3+。正确。
HCl+HClO,HCl是酸,电离产生H+使溶液显酸性,能使湿润的蓝色石蕊试纸变红,由于还产生了有强氧化性的HClO,它能把有色物质氧化为无色物质,所以后来又褪色。错误。C.在d处发生反应:Cl2+2NaOH=NaCl+NaClO+H2O。由于碱被消耗,溶液的碱性减弱,所以酚酞的红色逐渐变浅。错误。D.在e处发生反应:2Fe2++Cl2= 2Cl-+2Fe3+;Fe3++ 3SCN-=Fe(SCN)3.溶液变为血红色。证明了氧化性Cl2 > Fe3+。正确。
本题难度:一般
4、选择题 元素溴是1826年一位法国科学家发现的,它在研究海水制盐时,往剩余的副产物苦卤中通入氯气后发现溶液颜色变深,进一步提取,得到一种红棕色、有刺鼻臭味的液体,这种液体就是溴单质。只用溴水就可将下列各种溶液鉴别出来的是(?)
A.水、汽油、酒精
B.AgNO3、NaOH、KI
C.NaCl、NaBr、NaI
D.汽油、酒精、NaCl
参考答案:B
本题解析:A、D选项,只能通过分层检验出汽油。B选项中,溴水与AgNO3作用,生成淡黄色的AgBr沉淀;与NaOH溶液反应,生成无色的溴化钠、次溴酸钠和水,会观察到溴水褪色;与KI反应,置换出I2,溶液颜色加深,所以B选项可以鉴别。C选项只能鉴别出NaI。
本题难度:简单
5、选择题 浓盐酸和Ca(ClO)2能发生如下反应:Ca(ClO)2+4HCl(浓)= CaCl2 +2Cl2↑+2H2O,用贮存很久的漂白粉与浓盐酸反应制得的氯气中可能含有的杂质是
[? ]
①CO2? ②HCl? ③H2O? ④O2
A.①②③
B.②③④
C.只有②③
D.只有①④
参考答案:A
本题解析:
本题难度:一般