微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质均具有漂白作用,其中一种与另外三种的漂白原理不同的是( )
A.HClO
B.H2O2
C.SO2
D.O3
参考答案:C
本题解析:HClO、双氧水和臭氧的漂白性主要是这些物质的强氧化性的体现,而SO2则是与有色物质化合生成了不稳定的无色物质。?
本题难度:简单
2、选择题 下列说法不正确的是(?)
A.浓硝酸与足量铜片反应时,先生成红棕色气体,后生成无色气体
B.浓硫酸具有强氧化性,常温下可将铁、铝的单质氧化
C.饱和氯水既有酸性又有漂白性,加入NaHCO?后漂白性减弱
D.浓盐酸与足量二氧化锰反应后,盐酸有剩余
参考答案:C
本题解析:A.浓硝酸与足量铜片反应时,开始硝酸是浓度大的,浓硝酸和铜发生反应产生硝酸铜、二氧化氮和水;随着反应的进行。硝酸变稀,这时是铜与稀硝酸发生反应产生硝酸铜、一氧化氮和水。二氧化氮是红棕色的气体,一氧化氮是无色气体。所以先生成红棕色气体,后生成无色气体。正确。B.浓硫酸具有强氧化性,但常温下遇到铁、铝的单质因氧化产生致密的氧化物保护膜。产生钝化现象。正确。C.氯气溶于水得到氯水。氯气和水发生反应产生盐酸和次氯酸。这是个可能反应。含有氯气、次氯酸、盐酸。氯气、次氯酸有漂白性,盐酸有酸性,酸性比碳酸强。故加入NaHCO?消耗盐酸,破坏了电离平衡,使平衡正向移动。结果导致氯气浓度逐渐减小,次氯酸的浓度逐渐增大漂白性逐渐增强。错误。D.二氧化锰只和浓盐酸反应。随着反应的进行,盐酸变稀,这时就不再发生反应。所以盐酸有剩余。正确。
本题难度:一般
3、简答题 氯气是一种化学性质很活泼的单质,它具有较强的氧化性,下列叙述中不正确的是( )
A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟
B.氯气通入品红溶液中,溶液会褪色,是因为氯气具有漂白性
C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰
D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸
参考答案:A、因红热的铜丝在氯气里剧烈燃烧生成固体氯化铜,则会观察到棕黄色的烟,故A正确;
B、氯气通入品红溶液中,溶液会褪色,是氯气与水反应生成的HClO具有漂白性使其褪色,故B错误;
C、纯净的H2在Cl2中安静地燃烧生成HCl,观察到苍白色火焰,故C正确;
D、氯气能与水反应生成HClO和HCl,久置会发生2HClO?光照?.?2HCl+O2↑,则最终为稀盐酸,故D正确;
故选B.
本题解析:
本题难度:一般
4、填空题 已知CN- (氰根离子)、SCN- (硫氰酸根离子)和Cl-有相似之处:两个CN原子团或两个 SCN原子团可分别构成氰分子(CN)2和硫氰分子(SCN)2。(CN)2和(SCN)2的性质与Cl2的性质有相似之处,且常温、常压下是气体。写出下列反应的化学方程式:
(1)MnO2和HSCN溶液加热反应___________________________________。
(2)(CN)2和KOH溶液反应________________________________________。
(3)(SCN)2和AgNO3溶液反应______________________________________。
参考答案:(1)MnO2+4HSCN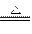 Mn(SCN)2+(SCN)2↑+2H2O
Mn(SCN)2+(SCN)2↑+2H2O
(2)(CN)2+2KOH====KCN+KCNO+H2O
(3)(SCN)2+H2O+AgNO3====AgSCN↓+HSCNO+HNO3
本题解析:(1)MnO2与浓盐酸的反应为:
MnO2+4HCl(浓)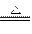 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
将“Cl”换作“SCN”即可。
(2)Cl2与KOH(aq)的反应为:
Cl2+2KOH====KCl+KClO+H2O
将“Cl”换作“CN”即可。
(3)Cl2通入AgNO3(aq)中,先与水反应:H2O+Cl2====HCl+HClO,生成的HCl再与AgNO3反应:HCl+AgNO3====AgCl↓+HNO3。总反应方程式:
Cl2+H2O+AgNO3====AgCl↓+HClO+HNO3
将“Cl”换作“SCN”即可。
本题难度:简单
5、填空题 氯气是一种重要的化工原料,除了用于消毒、制备盐酸和漂白剂外,还用于制备有机溶剂和农药。把氯气通入紫色石蕊溶液后,可以观察到的现象是_____________________________。请你解释其中的原因。
参考答案:溶液颜色应先变红,后逐渐褪为无色。因为氯气与水反应生成了盐酸和次氯酸:Cl2+H2O==HCl+HClO,溶液此时呈酸性使紫色石蕊溶液变红;因为生成的两种酸中有一种(次氯酸)具有漂白性,HClO把石蕊这种有机色质漂白,溶液红色又褪去。
本题解析:氯气通入紫色石蕊溶液后,溶液颜色应先变红,后逐渐褪为无色。这是因为氯气与水反应生成了盐酸和次氯酸:Cl2+H2O==HCl+HClO,溶液此时呈酸性使紫色石蕊溶液变红;因为生成的两种酸中有一种(次氯酸)具有漂白性,HClO把石蕊这种有机色质漂白,溶液红色又褪去。
本题难度:简单