��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� NA���������ӵ������������й�������ȷ����
A��1mol�������к���̼̼˫����Ϊ3NA
B��1mol�Ȼ�������к�H+ ������ΪNA
C��16 g CH4��18 g NH4+������������ΪNA
D��4.6 g����������ȫ��Ӧʧȥ������Ϊ0.2NA
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
2������� (8��)��10mL����AlO2�����ӵ���Һ����μ���1mol��L�����ᣬ ����Al(OH)3������������������������ϵ��ͼ��ʾ��
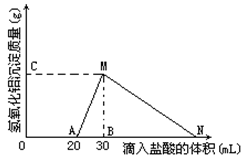
�ʣ�
(1)����Һ��ͬʱ����____mol___?���ӣ�
(2)�����ӷ���ʽ��ʾMN�η����ķ�Ӧ��?
(3)C(��M)���������Ϊ0.78����c(AlO2-)=?
(4)��B�ĺ�����Ϊ30����N�������HCl��Һ���Ϊ?mL
�ο��𰸣�(1)0.02mol;OH��? (2)Al(OH)3+3H+��Al3++3H2O
(3)1mol ?(4)60ml
�������������1����ͼ��֪���μ����Ὺʼ����������������Һ�л�����OH-����ʼ�����20mL���������к�OH-������H++OH-=H2O������Һ��n��OH-��=n��H+��=0.02L��1mol/L=0.02mol��
�ʴ�Ϊ��0.02��OH-��
��2����ͼ��֪��MN�����������������ᷴӦ�����Ȼ�����ˮ����Ӧ���ӷ���ʽΪAl��OH��3+3H+=Al3++3H2O��
�ʴ�Ϊ��Al��OH��3+3H+=Al3++3H2O��
��3����ͼ��֪����20mL��40mL�����ķ�ӦΪAlO2-+H++H2O�TAl��OH��3�����ý����ĵ��������Ϊ40mL-20mL=20mL���ɷ���ʽ��֪��Һ��n��AlO2-��=n��H+��=0.01L��1mol/L=0.01mol����c��AlO2-��=0.01mol/.0.01L=1mol/L��
�ʴ�Ϊ��1��
��4����ͼ��֪�������ᵽ��N������������ǡ����ȫ�ܽ⣬��ʱ��Һ��������ΪCl-�����ݵ���غ��֪n��Cl-��=n��AlO2-��+n��OH-��=0.01mol+0.02mol=0.03mol���ʴ˽����ĵ���������Ϊ0.03mol/1(mol/L) =0.03L=30mL����N������HCl��Һ�����Ϊ30mL+30mL=60mL��
�ʴ�Ϊ��60��
���������⿼�������仯��������ʡ��й�ͼ��Ļ�ѧ����ȣ��Ѷ��еȣ�������η����ķ�Ӧ�ǽ���Ĺؼ���ע��Ԫ�ػ�����֪ʶ�����ա�
�����Ѷȣ�һ��
3��ѡ���� ij�羰������Ϊ��Ȼ���ɣ���ԭ���ǿ����е����ɵ��Ӹ����ڷ��ӻ�ԭ�����γɿ��������ӣ�����Ϊ������ά���ء���O2-����һ�ֿ��������ӣ���Ħ������Ϊ
A��32 g
B��32 g��mol��1
C��33 g
D��33 g��mol��1
�ο��𰸣�B
���������Ħ�������ĵ�λ��g��mol��1���ų�AC��O2-��2����ͨ��ԭ�ӵ�Ħ������������B
�����Ѷȣ���
4��ѡ���� �������ʵ�����ͬ��CH4��CO2�Ƚϣ����н�����ȷ���ǣ�������
A�����Ӹ�����Ϊ5��3
B��̼ԭ�Ӹ�����Ϊ1��1
C�������Ϊ1��1
D��������Ϊ11��4
�ο��𰸣�B
���������
�����Ѷȣ���
5������� ����9�֣�
��1��0.5 mol H2O������Ϊ g�����к��� ��ˮ���ӣ����� ��ԭ�ӡ�
��2����������50 g�� HCl��NH3��CO2��O2���������У����з�����Ŀ���ٵ��� _ ������ͬ�¶Ⱥ���ͬѹǿ�����£���������� �������С���� ��
��3������50 mL 0.2 mol/L CuSO4��Һ����ҪCuSO4 g;��ҪCuSO4��5H2O _g��
��4���к���ͬ�������ͬ���ʵ���Ũ�ȵ�NaOH��Һ����ʹ���������Σ���Ҫ��ͬ���ʵ���Ũ�ȵ�HCl��H2SO4��H3PO4��Һ�������Ϊ ��
�ο��𰸣���1�� 9 3.01��1023 9.03��1023
��2�� CO2 NH3 CO2
��3�� 1.6 2.5 ��4�� 6
���������
�����Ѷȣ�һ��