微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是( )
实验
| 反应温度/℃
| Na2S2O3溶液
| 稀H2SO4
| H2O
|
V/mL
| c/(mol・L-1)
| V/mL
| c/(mol・L-1)
| V/mL
|
A
| 25
| 5
| 0.1
| 10
| 0.1
| 5
|
B
| 25
| 5
| 0.2
| 5
| 0.2
| 10
|
C
| 35
| 5
| 0.1
| 10
| 0.1
| 5
|
D
| 35
| 5
| 0.2
| 5
| 0.2
| 10
|
参考答案:D
本题解析:D项中反应温度最高,反应物Na2S2O3的浓度最大,反应速率最大,反应最先出现浑浊。
本题难度:一般
2、填空题 (15分)碳及其化合物有广泛的用途。
(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作?极。
(2)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)=CO(g)+H2(g);△H=+131.3kJ?mol-1,则要制备标准状况下22.4升水煤气,转移的电子的物质的量为?,需要吸收的热量为??kJ。
(3)工业上把水煤气中的混合气体经过处理后,获得的较纯H2用于合成氨:
N2(g)+3H2(g) 2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
2NH3(g);△H=-92.4kJ?mol-1。下图1是在两种不同实验条件下模拟化工生产进行实验所测得N2随时间变化示意图。
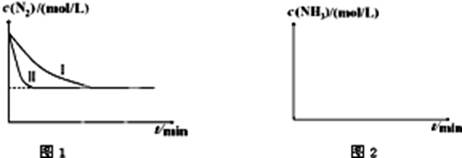
①与实验Ⅰ比较,实验Ⅱ改变的条件为:??。
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在上图2中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图。
(4)Na2CO3可在降低温室气体排放中用作CO2的捕捉剂。1L0.2mol/L Na2CO3溶液吸收标准状况下2.24LCO2后,溶液中各离子浓度由大到小的顺序为?。
参考答案:(1)正;?(2)1mol ;65.65KJ?;
(3)①使用催化剂?② ;(4)C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) 。
;(4)C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) 。
本题解析:(1)在电化学中,常用碳作电极。在碱性锌锰干电池中,碳棒作正极,Zn皮作负极。(2)根据反应方程式可知:每产生2mol的水煤气,转移电子2mol。现在要制备标准状况下22.4升水煤气,即制取1mol气体,所以转移的电子的物质的量为1mol;需要吸收的热量为131.3KJ÷2=65.65KJ;(3)①与实验Ⅰ比较,实验Ⅱ达到平衡所需要的时间缩短,但是平衡时物质的浓度没变,因此改变的条件为:使用催化剂。②若其它条件相同,实验Ⅲ比实验Ⅰ的温度要高,由于升高温度,化学反应速率加快,所以达到平衡所需要的时间缩短。但是由于该反应的正反应是放热反应,所以升高温度,平衡逆向移动,N2的平衡浓度增大,NH3的平衡浓度减小。故实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图为:
 。
。
(4)n(Na2CO3)= 1L×0.2mol/L=0.2mol;n(CO2)= 2.24L÷22.4L/mol=0.1mol.在溶液中发生反应:Na2CO3+H2O+ CO2= 2NaHCO3。由于二者反应时的物质的量的比为1:1,所以反应后的溶液含0.1mol的Na2CO3、0.2mol的NaHCO3。Na2CO3、NaHCO3都是强碱弱酸盐,水解使溶液显碱性,C(OH-)>C(H+)。但是盐的水解程度是微弱的,所以C(CO32-)>C(OH-)。故在溶液中离子浓度关系为C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) 。
本题难度:一般
3、选择题 实验室可利用反应“Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O”制取SO2,下列措施能降低该化学反应速率的是( )
A.适当降低反应温度
B.用铜粉代替铜片
C.加入MnO2作催化剂
D.将浓硫酸改为稀硫酸
参考答案:A、常温下铜与浓硫酸不反应,适当降低温度可以使化学反应速率减慢,故A正确;
B、用铜粉代替铜片,增大接触面积,加快反应速率,故B错误;
C、加入MnO2对该反应没有影响,故C错误;
D、铜与稀硫酸不反应,不能生成二氧化硫,故D错误.
故选A.
本题解析:
本题难度:一般
4、选择题 加入正催化剂使反应速率加快,下列叙述不正确的是( )
A.使反应体系的活化能降低
B.使反应体系的活化分子总数增多
C.使正反应速率增大,逆反应速率减小
D.使反应体系的活化分子百分数增大
参考答案:A、加入正催化剂使反应体系的活化能降低,进而使反应速率加快,故A正确;
B、正催化剂使反应体系的活化分子总数增多,故B正确;
C、催化剂能同等程度的改变正逆反应速率,加入正催化剂使正反应速率增大,逆反应速率也增大,故C错误;
D、催化剂可以使反应体系的活化分子百分数增加,故D正确.
故选C.
本题解析:
本题难度:一般
5、选择题 下列措施中,能加快化学反应速率的是
A.将食物储存在冰箱里
B.在稀H2SO4与NaOH溶液反应时,增大压强
C.往H2O2溶液中加入几滴FeCl3溶液
D.用18mol/L H2SO4溶液代替1 mol/L H2SO4溶液与铁反应
参考答案:C
本题解析:在其它条件不变的情况下,升高温度或增大反应物的接触面积或使用催化剂等均可以加快反应速率,据此可知选项C能加快反应速率。A中降低反应速率,B中压强对反应速率的影响不能适用于液体,D中浓硫酸和铁在常温下发生钝化,答案选C。
点评:该题是中等难度的试题,主要是考查学生对外界条件是如何影响反应速率的了解掌握情况,意在培养学生的逻辑推理能力,提高学生的应试能力。该题需要注意的是压强对反应速率的影响适用范围。
本题难度:一般