��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ӷ���ʽ��д��ȷ����
A������ˮ�⣺S2����2H2O  H2S����2OH��
H2S����2OH��
B��̼�������ڴ�����Һ�У�CO32���� 2 H���� H2O �� CO2��
C�����������Һ��ͨ�����������̼��Ca2+ + 2ClO��+H2O+CO2��CaCO3��+2HClO
D����������������������������Һ��Ӧ��Ba2����2OH����2H����SO42����BaSO4����2H2O
�ο��𰸣�D
���������
��ȷ�𰸣�D
A������ȷ�����Ʒֲ�ˮ�⣺S2����H2O  ?HS�D��OH��
?HS�D��OH��
B������ȷ��̼�������ڴ�����Һ�У�CO32���� 2 CH3COOH��2H2O �� CO2����2CH3COO�D
C������ȷ�����������Һ��ͨ�����������̼�� ClO��+H2O+CO2��HCO3�D +HClO
D.��ȷ��
�����Ѷȣ�һ��
2��ѡ���� ������ȷ��ʾ���л�ѧ��Ӧ�����ӷ���ʽ�ǣ�������
A��̼��Ƹ����ᷴӦ��CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2��
B��̼������������У�CaCO3+2H+=H2O+CO2��+Ca2+
C��������ϡ�����У�Al+2H+=Al3++H2��
D��FeSO4��Һ�м����������ữ��H2O2��Һ��2Fe2++2H++H2O2=2Fe3++2H2O
�ο��𰸣�A��̼��Ƹ����ᷴӦ�����ӷ�ӦΪCaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2������A��ȷ��
B��̼������������е����ӷ�ӦΪCaCO3+2H+=H2O+CO2��+Ca2+����B��ȷ��
C��������ϡ�����е����ӷ�ӦΪ2Al+6H+=2Al3++3H2������C����
D��FeSO4��Һ�м����������ữ��H2O2��Һ�����ӷ�ӦΪ2Fe2++2H++H2O2=2Fe3++2H2O����D��ȷ��
��ѡC��
���������
�����Ѷȣ�һ��
3��ѡ���� ���н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ��ȷ���ǣ�������
A����ʳ�׳�ȥůˮƿ�е�ˮ����2CH3COOH+CaCO3�TCa2++2CH3COO-+CO2��+H2O
B������ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2��
C��ϡ�����м������ۡ�2Fe+6H+�T2Fe3++3H2��
D��Ca��HCO3��2��Һ�м���������NaOH��Һ��Ca2++2HCO
+2OH-�TCaCO3��+CO+2H2O
�ο��𰸣�A����ʳ�׳�ȥůˮƿ�е�ˮ������Ӧʵ��Ϊ������̼��Ƶķ�Ӧ����Ӧ�����ӷ���ʽΪ��2CH3COOH+CaCO3�TCa2++2CH3COO-+CO2��+H2O����A��ȷ��
B������ˮ��Ӧ�����������ƺ������������ӷ���ʽ��ɲ��غ㣬��ȷ�����ӷ���ʽΪ��2Na+2H2O�T2Na++2OH-+H2������B����
C��ϡ�����м������۷�Ӧ�����������Ӻ���������ȷ�����ӷ���ʽΪ��2Fe+2H+�TFe2++H2������C����
D����������������̼��������Ӳ��ִ��ڣ���ȷ�����ӷ���ʽΪ��Ca2++HCO3-+OH-�TCaCO3��+H2O����D����
��ѡA��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A���������ƺ�ˮ��Ӧ��2Na2O2+2H2O�T4Na++4OH-+O2��
B����ͭΪ�缫��ⱥ��ʳ��ˮ��2Cl-+2H2O
Cl2��+H2��+2OH-
C����������Һ�еμӹ�����ˮ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+
D����С�մ���Һ�м�����Ba��OH��2��Һ��HCO3-+Ba2++OH-�TBaCO3��+H2O
�ο��𰸣�A���������ƺ�ˮ��Ӧ�����ӷ�ӦΪ2Na2O2+2H2O�T4Na++4OH-+O2������A��ȷ��
B����ͭΪ�缫��ⱥ��ʳ��ˮ�����ӷ�ӦΪCu+2H2Oͨ��.Cu��OH��2��+H2������B����
C����������Һ�еμӹ�����ˮ�����ӷ�ӦΪAl3++3NH3?H2O�TAl��OH��3��+3NH4+����C��ȷ��
D����С�մ���Һ�м�����Ba��OH��2��Һ�����ӷ�ӦΪ2HCO3-+Ba2++2OH-�TBaCO3��+2H2O+CO32-����D����
��ѡAC��
���������
�����Ѷȣ�һ��
5������� �ס��ҡ����Ƿֱ���H��C��O��Si��Al��Cu������Ԫ���е����ֻ����Ԫ����ɵĻ������֪�ס��ҡ����������ᾧˮ����������Ŀ����ǹ�ҵ�ϵ�ⷨұ��ij�ֳ����������ʵ�ԭ�ϣ���������һ�ָ��۵㻯���������ǿ�ᡢǿ����Һ�����������ǹ��ά����Ҫ�ɷ֣��������Ϊһ�ֳ�����ɫ�ļ�ʽ�Σ���34.6g�������������ȷֽ�����24g��ɫ����X����ɫ��������Y����״���£��ܶ�Ϊ1.96g/L����ˮ�����ɵ�Y�ۺϳɱ�״���µ����Ϊ4.48L������X������ˮ�����������ᣬ�γ���ɫ��Һ����ش��������⣺
��1��д������Y�Ľṹʽ______����������Ļ�ѧʽ______��
��2��д������NaOH��Һ��Ӧ�����ӷ���ʽ______�����⣬��ҵ�ϳ��ü��뽹̿�������������ɻ����ﶡ��CO��������������Ԫ����ɣ���д���÷�Ӧ�Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ______��
��3������������������һ�ּ�ǿ�Ķ�Ԫ���ˮ��������������3��Ԫ����ɣ����з�Ԫ�ص���������Ϊ79.17%����д�����������������ӷ�Ӧ����ʽ______��
��4��������X�������������ᣬ��������Һ�еμ�NaOHŨ��Һʱ���ȳ�����ɫ��״�����������μ�NaOHŨ��Һ���������������ʧ�γ���ɫ��Һ�����ٵμ������Ҷ������ɹ۲쵽��Һ�����ɫ���ɼ�������ɫ��״���������______��
A������?B������?C������?D��ǿ��ԭ��
��д�����Ҷ�����Ӧ�Ļ�ѧ����ʽ������Ӧ������ɫ��״������Ļ�ѧʽ��ʾ��______��
�ο��𰸣��ס��ҡ����Ƿֱ���H��C��O��Si��Al��Cu������Ԫ���е����ֻ����Ԫ����ɵĻ����
��������Ŀ����ǹ�ҵ�ϵ�ⷨұ��ij�ֳ����������ʵ�ԭ�ϣ���������һ�ָ��۵㻯���������ǿ�ᡢǿ����Һ��������ʺ��е�Ԫ�أ���ΪAl2O3��
���������ǹ��ά����Ҫ�ɷ֣���ΪSiO2��
�������Ϊһ�ֳ�����ɫ�ļ�ʽ�Σ���34.6g�������������ȷֽ�����24g��ɫ����X����ɫ��������Y����״���£��ܶ�Ϊ1.96g/L����ˮ��Y��Ħ������Ϊ1.96g/L��22.4L/mol=44g/mol��������ʺ��е�Ԫ�أ���YΪCO2������X������ˮ�����������ᣬ�γ���ɫ��Һ��Ϊ����ͭ��Һ����XΪCuO������Ϊ��ʽ̼��ͭ�����ɵ�CO2�ۺϳɱ�״���µ����Ϊ4.48L�����ʵ���Ϊ4.48L22.4L/mol=0.2mol������̼Ԫ���غ��֪CuCO3Ϊ0.2mol��24gCuO�����ʵ���Ϊ24g80g/mol=0.3mol������ͭԪ���غ�Cu��OH��2Ϊ0.3mol-0.2mol=0.1mol���ʼ�ʽ̼��ͭ��n��CuCO3����n[Cu��OH��2]=0.2mol��0.1mol=2��1���ʸü�ʽ̼��ͭ��ѧʽΪ2CuCO3?Cu��OH��2��
��1��������������֪��YΪCO2��������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ��ṹʽΪO=C=O���������Ϊ2CuCO3?Cu��OH��2��
�ʴ�Ϊ��O=C=O��2CuCO3?Cu��OH��2��
��2����ΪAl2O3��Al2O3��NaOH��Һ��Ӧ����ƫ��������ˮ����Ӧ���ӷ���ʽΪ��Al2O3+2OH-=2AlO2-+H2O��
?��ҵ�ϳ���Al2O3�뽹̿�������������ɻ����ﶡ��CO��������������Ԫ����ɣ���Ԫ���غ��֪��ΪAlCl3����Ӧ����ʽΪAl2O3+3C+3Cl2?����?.?3CO+2AlCl3��CԪ�ػ��ϼ���0������Ϊ+2��ʧȥ������Ϊ6����Ԫ�ػ��ϼ���0�۽���Ϊ-1�ۣ���õ�����ĿΪ6���������ת�Ƶķ������ĿΪ��
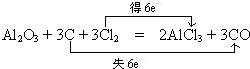
��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��

��
��3��SiO2��������������һ�ּ�ǿ�Ķ�Ԫ���ˮ��������3��Ԫ����ɣ����з�Ԫ�ص���������Ϊ79.17%��������Hԭ����ĿΪ2�������Ļ�ѧʽΪ��H2SixFy�����ݻ��ϼ۴�����Ϊ0��֪2+4x-y=0���ɷ�Ԫ������������19y2+28x+19y=79.17%���������x=1��y=6���ʸ���ΪH2SiF6����SiO2�������������ӷ�Ӧ����ʽΪ��SiO2+6HF=2H++SiF62-+2H2O��
�ʴ�Ϊ��SiO2+6HF=2H++SiF62-+2H2O��
��4��������CuO�������������ᣬ��������Һ�еμ�NaOHŨ��Һʱ���ȳ�����ɫ��״������ΪCu��OH��2�������μ�NaOHŨ��Һ���������������ʧ�γ���ɫ��Һ��˵��Cu��OH��2�������ԣ��ٵμ������Ҷ������ɹ۲쵽��Һ�����ɫ���ǻ�������λ�Ķ�Ԫ������ǻ����������������ͭ������Ϸ�Ӧ������ɫ��Һ����Ӧ����ʽΪ��
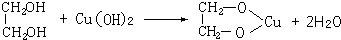
��
�ʴ�Ϊ��C��

��
���������
�����Ѷȣ�һ��