微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于电解KNO3溶液时的叙述正确的是
A. 向阴极移动,K+向阳极移动,分别在对应的极上析出
向阴极移动,K+向阳极移动,分别在对应的极上析出
B.随电解的进行,溶液的pH减小
C.OH-向阳极移动,阳极附近溶液显碱性
D.阴极上H+得电子被还原成H2,促进水的电离平衡正向移动,富集下来的OH-使得阴极附近溶液呈碱性
参考答案:D
本题解析:根据电解原理,溶液中的阴离子 、OH-定向向阳极移动后,OH-失电子被氧化生成O2,因而阳极区OH-浓度迅速减小,使得c(H+)>c(OH-),故阳极附近溶液显酸性;另溶液中的阳离子K+、H+定向向阴极移动后,H+得电子生成H2,因而使得阴极区H+浓度迅速减小,使得c(OH-)>c(H+),故阴极附近溶液显碱性。
、OH-定向向阳极移动后,OH-失电子被氧化生成O2,因而阳极区OH-浓度迅速减小,使得c(H+)>c(OH-),故阳极附近溶液显酸性;另溶液中的阳离子K+、H+定向向阴极移动后,H+得电子生成H2,因而使得阴极区H+浓度迅速减小,使得c(OH-)>c(H+),故阴极附近溶液显碱性。
本题难度:简单
2、实验题 已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
AsO33-+I2+H2O是可逆反应。现设计如下图所示实验装置(装置中盐桥的作用是使整个装置形成一个闭合的回路)进行下述操作:
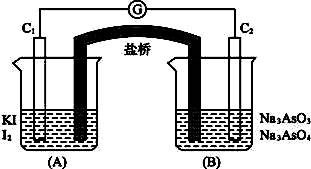
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现微安表指针偏转;
(Ⅱ)若改向(B)烧杯中滴加40%NaOH溶液,发现微安表指针偏转方向与Ⅰ相反。
试完成下列问题:
(1)两次操作过程中微安表指针为什么会发生偏转?
(2)两次操作过程中指针偏转方向为什么相反?
参考答案:(1)两次操作均发生原电池反应,电流表指针偏转,化学能转变为电能。
(2)由于c(H+)改变,使化学平衡向不同方向移动发生不同方向的反应。
本题解析:Ⅰ.操作过程中,C1棒发生的反应为2I--2e-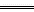 I2
I2
Ⅱ.操作过程中,C2棒发生的反应为AsO33-+H2O-2e-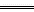 AsO43-+2H+
AsO43-+2H+
总反应为AsO43-+2I-+2H+ AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。
AsO33-+I2+H2O,Ⅰ操作中I-被氧化,AsO43-被还原;Ⅱ操作中AsO43-被氧化,I2被还原。
Ⅰ操作中(A)池发生氧化反应C1为负极;(B)池中发生还原反应C2为正极。
Ⅱ操作中(A)池发生还原反应C1为正极;(B)池中发生氧化反应C2为负极。
本题难度:一般
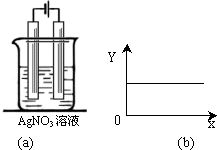
3、选择题 按图a中装置进行实验,图中两电极均为银棒,若图b的X轴表示流入电极的电子的量,则Y轴不可能表示的情况是( )
A.c(Ag+)
B.c(NO3-)
C.溶液的pH
D.银棒质量