微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6mol/L NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片用水冲洗、烘干后称量,得质量为m2。下列说法正确的是
[? ]
A.设锌镀层厚度为,锌的密度为,则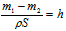
B.锌电极上发生还原反应
C.锌和石墨形成原电池,外电路中电流从锌流向石墨
D.当石墨不再产生气泡时,应立即取出铁皮
参考答案:D
本题解析:
本题难度:一般
2、选择题 关于原电池和电解池的叙述正确的是( )
A.原电池中失去电子的电极为阴极
B.原电池的负极、电解池的阳极都发生氧化反应
C.原电池的两极一定是由活动性不同的两种金属组成
D.电解时电解池的阴极一定是阴离子放电
参考答案:A、原电池中失去电子的电极为负极不是阴极,故A错误;
B、原电池负极上失电子发生氧化反应,电解池阳极上失电子发生氧化反应,故B正确;
C、原电池的两极不一定是由活动性不同的两种金属组成,可能是由金属和导电的非金属组成,故C错误;
D、电解时,电解池阴极上得电子发生还原反应,故D错误.
故选B.
本题解析:
本题难度:简单
3、选择题 某原电池反应的离子方程式为:Fe+2H+=Fe2++H2↑,则下列说法正确的是(?)
A.HNO3为电解质溶液
B.锌为原电池正极
C.铁极质量不变
D.铜为原电池正极
参考答案:D
本题解析:由电池反应的离子方程式知,负极为铁,则正极应是比铁不活泼的金属,B选项错。在反应中负极不断被消耗,C选项错。由于反应放出了氢气并生成了Fe2+,故知电解质溶液不能是HNO3。由上分析可知正确选项为D。
本题难度:一般
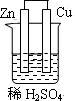
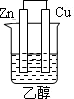
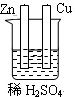
4、选择题 下列为原电池装置的是
 ?
? ?
? ?
?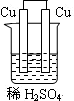
A? B? C? D
参考答案:A
本题解析:考查原电池的构成,构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连并插入到电解质溶液中,所以A正确。B中乙醇是非电解质,C中没有用导线相连,D中电极是同一种金属,且和稀硫酸不反应,答案选A。
本题难度:一般
5、选择题 如图所示,先闭合S1,打开S2一段时间后,下列操作或现象描述正确的是( )
A.闭合S1,打开S2,经过一段时间,溶液的物质的量浓度会减小
B.闭合S1,打开S2时,甲为阳极,乙为阴极
C.闭合S2,打开S1时,甲为负极,乙为正极
D.闭合S2,打开S1时,电能转化为光能,二极管发光