微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
?压强/MPa
转化率/%
温度/℃?
| 0.1
| 0.5
| 1
| 10
|
400
| 99.2
| 99.6
| 99.7
| 99.9
|
500
| 93.5
| 96.9
| 97.8
| 99.3
|
600
| 73.7
| 85.8
| 89.5
| 96.4
|
?
(1)已知SO2的氧化是放热反应,如何利用表中数据推断此结论?________________________________________________________。
(2)在400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:__________________________________________。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?________(填“是”或“否”),是否可以增大该反应放出的热量?________(填“是”或“否”)。
(4)为提高SO3吸收率,实际生产中用________吸收SO2。
(5)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.9 kJ・mol-1,计算每生产1万吨98%的硫酸所需要的SO3质量和由SO2生产这些SO3所放出的热量。
参考答案:(1)压强一定时,温度升高时,SO2转化率下降,说明升温有利逆反应的进行,所以正反应为放热反应
(2)增大压强对提高SO2转化率无显著影响,反而会增加成本
(3)否 ?否
(4)浓硫酸
(5)8.0×103 t 9.845×109 kJ
本题解析:(1)根据表格中的数据可以看出,在相同压强下(如在0.1 MPa下)升高温度(如由400℃升高到500℃)时SO2的转化率降低(由99.2%降低为93.5%),即升高温度时此化学平衡向逆反应方向移动,而升高温度化学平衡应该向吸热反应方向移动,所以此反应的正反应为放热反应。
(2)根据表格中的数据可以得知:在0.1MPa下SO2的转化率已经很高,如在400℃时已达99.2%,若增大压强到10 MPa,压强增大了100倍但是SO2的转化率增大为99.9%,只增大了0.7%,变化不大。而压强增大100倍,需要对设备的材料、动力、能源等都做相应地提高,增大成本投入。
(3)使用催化剂只能改变化学反应的速率,改变反应到达平衡的时间,不能使化学平衡发生移动,即对SO2的转化率不产生影响;而在一定条件下,化学反应放出的热量与参加反应的反应物的量成正比,因SO2的转化率不变,所以反应放出的热量也不会增大。
(4)在生产实际中是采用98.3%的浓硫酸作吸收剂来吸收SO3的。因为若用水进行吸收会形成酸雾,将影响SO3的吸收速率和效率。
(5)1万吨98%的硫酸含H2SO4的质量:9.8×109 g。
设需要SO3的质量为x,该反应产生的热量为y。
H2SO4~ SO3~ 放出的热量
98 g?80 g?196.9 kJ×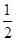
9.8×109 g? x?y
则 =
=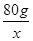 =
=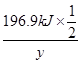 ,
,
解得x=8.0×103 t,y=9.845×109 kJ。
本题难度:一般
2、选择题 下列生产工艺不能体现“绿色化学”或环保思想的是
[? ]
A.海水提镁:用电解氯化镁产生的氯气制取盐酸
B.工业制硫酸:提高尾气排放的烟囱高度
C.工业制胆矾:使用稀硫酸、双氧水溶解铜
D.火力发电:在燃煤中加入适量生石灰
参考答案:B
本题解析:
本题难度:简单
3、填空题 (8分)【化学-化学与技术】
工业上合成氨是在一定条件下进行如下反应:N2(g)+3H2(g) 2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
2NH3(g);△H=-92.44 kJ/mol;其部分工艺流程如下:
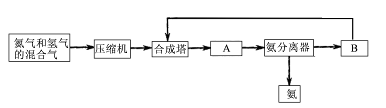
(1)合成氨所需要的原料气中,氮气取自?,氢气来源于?。
(2)对原料气进行净化处理的目的是?。
(3)设备A的名称是??,设备B的名称是??。
(4)在10~30Mpa时,工业合成氨选择400~500 ℃的温度进行反应,主要原因是?。
(5)据《科学》杂志报道,希腊化学家在常压下将氢气和用氢气稀释的氮气分另通入一个加热到570 ℃的电解池(如图)中,氢和氮在电极上合成了氨,且转化率达到了78%。
则阳极反应为?,阴极反应为?。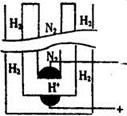
参考答案:⑴空气(1分)?水和碳氢化合物(1分)?⑵防止催化剂中毒(1分)
⑶冷凝器(1分)?循环压缩机(1分)
⑷温度500 ℃是因为温度太高,平衡混合物中氨的含量太低;温度太低,则化学反应速率太小。而且500 ℃,催化剂活性最大。(1分)
⑸H2-2e-=2H+(1分)? N2+6e-+6H+=2NH3(1分)
本题解析:⑴空气的主要成分是氮气,所以合成氨所需要的原料气中,氮气取自空气。而氢气来源于水和碳氢化合物。
⑵原料气中含有杂质,如果不处理会造成催化剂中毒,所以对原料气进行净化处理,是为了防止催化剂中毒。
⑶设备A为冷凝器,设备B为循环压缩机。
⑷选择400~500 ℃的温度,是综合反应速率、反应限度及催化剂活性等考虑。因为温度太高,平衡混合物中氨的含量太低;温度太低,则化学反应速率太小。而且500 ℃,催化剂活性最大。
⑸该装置为电解池,阳极失去电子,所以氢气在阳极通入,阳极反应为H2-2e-=2H+,阴极得到电子,因此氮气在阴极通入,所以阴极反应为N2+6e-+6H+=2NH3。
本题难度:一般
4、选择题 下列叙述正确的是
[? ]
A.通过沉淀反应,可以使溶液中被沉淀离子的浓度为零
B.化学反应过程中,一定有化学键的断裂和形成
C.若测得雨水的pH小于7,则下的是酸雨
D.在通风橱中进行有毒气体实验符合“绿色化学”思想
参考答案:B
本题解析:
本题难度:简单
5、选择题 “绿色化学”是当今社会提出的一个新概念.在“绿色化学工艺”中,理想状态是反应中原子全部转化为欲制得产物,即原子的利用率为100%.在用丙炔合成甲基丙烯酸甲酯
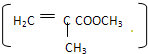
的过程中,欲使原子的利用率达到最高,在催化剂作用下还需要其他的反应物是( )
A.CO和CH3OH
B.CO2和H2O
C.CH2=CH2和CO
D.CH3OH和H2
参考答案:A
本题解析:
本题难度:简单