微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 等物质的量的下列化合物在相应条件下完全分解后得到氧气最多的是( )
A.KClO3(加MnO2催化剂,加热)
B.KMnO4加热
C.H2O2(水溶液,加MnO2催化剂)
D.HgO(加热)
参考答案:A
本题解析:
本题难度:简单
2、选择题 将6.72L(标准状况)乙烯与乙烷的混合气体通入足量的溴水中,充分反应后,溴水的质量增加了2.8g,则原气体混合物中乙烯与乙烷的物质的量之比是( )
A.1:2
B.2:1
C.1:3
D.3:1
参考答案:6.72L混合气体的物质的量为n=VVm=6.72L?22.4L/mol?=0.3mol,乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,即为乙烯的质量,所以乙烯的物质的量为n=5.6g?28g/mol?=0.2mol,则乙烷的物质的量为:0.3mol-0.2mol=0.1mol,所以,乙烯与乙烷的物质的量之比为0.2mol:0.1mol=2:1,
故选B.
本题解析:
本题难度:简单
3、简答题 完成下列反应的化学方程式:
(1)苯制备硝基苯______
(2)丙烯的加聚______
(3)将乙烯通入溴的四氯化碳溶液中______
(4)甲苯完全燃烧生成CO2和H2O______
(5)乙醇跟浓硫酸加热反应生成二氧化硫、二氧化碳、一氧化碳、水蒸气和炭黑,测得n(CO2):n(CO):n(C)=1:1:1
______.
参考答案:(1)苯和浓硝酸之间发生取代反应生成硝基苯的化学方程式为:
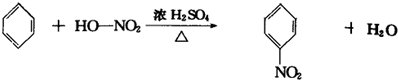
,
故答案为:
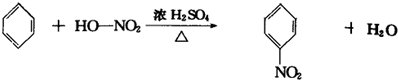
;
(2)烯烃能发生加聚反应,丙烯的加聚方程式为:
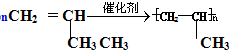
,
故答案为:
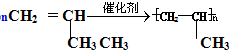
;
(3)含有双键的烯烃可以断开双键中的一个键而发生加成反应,乙烯和溴单质的加成反应为:
CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(4)烃燃烧生成物是水和二氧化碳,甲苯燃烧的方程式为:C7H8+9O2?点燃
本题解析:
本题难度:一般
4、简答题 将1.12L标准状况下由X、Y组成的混合气体用水全部吸收得到1L溶液,测得pH=1,则X、Y可能是( ),X与Y的体积比为( )
A.H2,Cl2;1:1
B.NO2,O2;4:1
C.Cl2,SO2;1:1
D.NO,O2;4:3
参考答案:A、H2,Cl2的混合气体,用水吸收,氢气不能被吸收,混合气体不能全部吸收,故A错误;
B、NO2与O2按4:1混合,发生反应4NO2+O2+2H2O=4HNO3,气体全部被吸收,1.12L标准状况下该混合气体的物质的量为0.05mol,所以NO2与O2分别为0.04mol、0.01mol,由方程式可知生成HNO30.04mol,所以溶液中c(H+)=0.04mol/L,不是0.1mol/L,故B错误;
C、Cl2与SO2按1:1混合,发生反应Cl2+SO2+2H2O=2HCl+H2SO4,气体全部被吸收,1.12L标准状况下该混合气体的物质的量为0.05mol,所以Cl2与SO2分别为0.025mol、0.025mol,由方程式可知生成HCl0.05mol,生成H2SO40.025mol,所以溶液中c(H+)=0.05mol+0.025mol×21L=0.1mol/L,故C正确;
D、NO与O2按4:3混合,发生反应4NO2+3O2+2H2O=4HNO3,气体全部被吸收,1.12L标准状况下该混合气体的物质的量为0.05mol,所以NO与O2分别为47×0.05mol、37×0.05mol,由方程式可知生成HNO347×0.05mol,所以溶液中c(H+)=47×0.05mol/L=0.029mol/L,不是0.1mol/L,故D错误.
故选:C.
本题解析:
本题难度:一般
5、选择题 下列反应中转移电子的物质的量不等于2 mol的是
A.1 mol Al与含1mol H2SO4的稀硫酸溶液反应
B.1mol Cu与含4mol HNO3的稀硝酸溶液反应
C.1 mol MnO2与含2 mol H2O2的双氧水反应
D.1 mol Cu与含2 mol H2SO4的浓硫酸共热
参考答案:D
本题解析:A ,Al与硫酸反应的化学方程式为:2Al+3H2SO4=Al2(SO4)3+3H2↑.可见Al过量。反应按照硫酸来计算。硫酸是1mol,所以发生反应转移电子2mol。正确。B.Cu与稀 HNO3反应的化学方程式为: 3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O,可见1mol Cu与消耗8/3mol HNO3.。因此硝酸过量。按照Cu来计算。Cu是+2价的金属,1mol的 Cu转移电子2mol。正确。C.1 mol MnO2与含2 mol H2O2的双氧水反应反应的方程式为2H2O2 2H2O +O2↑.2 mol H2O2发生分解反应作用电子2mol。正确。D.1 mol Cu与含2 mol H2SO4的浓硫酸共热Cu+2H2SO4(浓)
2H2O +O2↑.2 mol H2O2发生分解反应作用电子2mol。正确。D.1 mol Cu与含2 mol H2SO4的浓硫酸共热Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。1mol的Cu发生反应,消耗2mol的硫酸。随着反应的进行,硫酸变稀,这时反应就不再发生。因此转移电子的物质的量小于2mol。
CuSO4+SO2↑+2H2O。1mol的Cu发生反应,消耗2mol的硫酸。随着反应的进行,硫酸变稀,这时反应就不再发生。因此转移电子的物质的量小于2mol。
本题难度:一般