| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《物质的量》高频试题特训(2017年最新版)(二)
参考答案:D 本题解析:A、未指明标准状况,所以0.5mol Cl2所占体积不一定为11.2 L,错误;B、16g氧气的物质的量是16g/32g/mol=0.5mol,所以0.5mol氧气中的分子数是6.02×1023×0.5=3.01×1023,错误;C、氯化钠溶液的体积未知,所以氯化钠的物质的量无法计算,错误;D、标准状况下11.2LN2和CO的混合气体的物质的量是11.2L/22.4L/mol=0.5mol,N2和CO都是双原子分子,所以含有的原子数是6.02×1023×0.5×2=6.02×1023,正确,答案选D。 本题难度:一般 2、选择题 下列有关阿伏加德罗常数(NA)的说法错误的是(? ) 参考答案:C 本题解析:考查阿伏加德罗常数的应用。32g氧气的物质的量是1mol,所以含有2mol氧原子,选项A正确;SO2是由1个S原子和2个氧原子构成的,共计含有3个原子,所以0.5molSO2含有的原子数目为1.5NA,选项B正确;选项C不正确,0.5molSO2含有的分子数目为0.5NA;根据 本题难度:一般 3、选择题 下列对于“摩尔”的理解正确的是 |
参考答案:D
本题解析:A、物质的量是国际科学界建议采用的一种物理量,单位是mol,错误;B、2H只表示2个氢原子不可表示2 mol氢分子,错误;C、氧是分子还是原子,叙述不明确,错误;D、摩尔是物质的量的单位,简称摩,符号为mol,正确,故选D。
考点:考查物质的量的单位与物理量之间的关系。
本题难度:一般
4、计算题 取标准状况下CH4和过量O2的混合气体840 mL点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0. 600 g。 计算:
(1)碱石灰吸收后所剩气体的体积(标准状况下);
(2)原混合气体中CH4与O2的体积比。
参考答案:(1) CH4 +2O2 CO2+2H2O,1 mol CH4完全燃烧得到的CO2和H2O共80 g,
CO2+2H2O,1 mol CH4完全燃烧得到的CO2和H2O共80 g,
原混合气体中n(CH4)=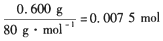 ,
,
CH4的体积为0.0075 mol×22.4× 103 mL/mol=168 mL,
剩余气体的体积=840 mL-3×168 mL =336 mL,
(2)V(CH4):V(O2)=168 mL:( 840 mL - 168 mL) =168 mL:672 mL=1:4
本题解析:
本题难度:一般
5、选择题 下列说法正确的是( )
A.在常温常压下,11.2 L氧气含有的分子数为0.5NA
B.在常温常压下,1 mol He含有的原子数为NA
C.32g氧气含原子数目为NA
D.在同温同压下,相同体积任何气体单质所含的原子数目相同
参考答案:B
本题解析:常温常压下,11.2L氧气的物质的量不是0.5mol,选项A不正确;氦气是1各原子构成的,选项B正确;氧气是2各氧原子构成的,所以32g氧气含有2mol氧原子,选项C不正确;在同温同压下,相同体积任何气体单质所含的分子数目相同,原子数不一定相等,选项D不正确,答案选B。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《吸热反应与.. | |