��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������Ż�ʱ����������������
A.ˮ
B.ɰ��
C.ú��
D.������̼
�ο��𰸣�B
�����������B��
�������Ż�ʱ������B��ɰ�����A��ˮ��Na��Ӧ��C��ú����ȼ��?D��������̼��֧����ȼ�ա�
�����Ѷȣ�һ��
2��ѡ���� ������Һ����þ��Ӧ������������
A.�Ȼ����Һ
B.����������Һ
C.̼�����Һ
D.����ʯ��ˮ
�ο��𰸣�A
�������������������þ�Ľ���ǿ��ǿ�����Ժ������ˮ�������Ե�����Һ��Ӧ����������
���A���Ȼ���е�笠�����ˮ�������ԣ����Ժͽ���þ��Ӧ������������A��ȷ��
B���������ƺͽ���þ����Ӧ����B����
C��̼������Һ��̼�������ˮ���Լ��ԣ����ܺͽ���þ��Ӧ����C����
D������ʯ��ˮ�Լ��ԣ��������þ��Ӧ����D����
��ѡA��
���������⿼��ѧ������þ�Ļ�ѧ���ʣ���������ijЩ���ӵ�ˮ�������Һ�еIJ����������ǽ����Ĺؼ����ѶȲ���
�����Ѷȣ�һ��
3��ѡ���� ���и����ʲ�����CO2��Ӧ����
��Li2O? ��Na2O2? ��Na2CO3��Һ? ��NaHCO3��Һ ? ��Ca��OH��2��Һ ? ��CaCl2��Һ
A.�٢ۢ�
B.�ڢݢ�
C.�ܢ�
D.�٢�
�ο��𰸣�C
����������٢���CO2��Ӧ�ֱ�����Li2CO3��Na2CO3��O2������CO2��Ӧ����NaHCO3�����Ǽ���CO2��������Ӧ��
�����Ѷȣ�����
4��ѡ���� 9.2g������Ͷ�뵽��������ˮ�У�������������к���
A.0.2?mol����
B.0.4?mol����
C.0.2?mol����
D.0.4?mol����
�ο��𰸣�B
������������������ݷ�Ӧ2Na+22H2O=2NaO2H+2H2����n��Na��=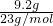 =0.4mol����ϻ�ѧ����ʽ��ԭ�ӵĹ��ɼ��㣮
=0.4mol����ϻ�ѧ����ʽ��ԭ�ӵĹ��ɼ��㣮
���n��Na��=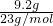 =0.4mol��
=0.4mol��
��Ӧ����ʽΪ2Na+22H2O=2NaO2H+2H2����
����n��2H2��=0.2mol����
A������Ϊ0.2mol��2=0.4mol����A����
B������Ϊ0.2mol��2=0.4mol����B��ȷ��
C������Ϊ0.2mol��2=0.4mol����C����
D������Ϊ0.2mol����D����
��ѡB��
���������⿼�黯ѧ��Ӧ�ļ��㣬��Ŀ�ѶȲ�����Ҫ�ر�ע�����ԭ�ӵĹ��ɣ�
�����Ѷȣ���
5��ѡ���� ��5.4g?AlͶ��200.0mL?2.0mol?L-1��ij��Һ����������������ַ�Ӧ���н���ʣ�࣮����Һ����Ϊ
A.HNO3��Һ
B.Ba��OH��2��Һ
C.H2SO4��Һ
D.HCl��Һ
�ο��𰸣�D
���������������200.0mL?2.0mol?L-1��ij��Һ�����ʵ����ʵ���Ϊ0.2L��2.0mol?L-1=0.4mol��Al�����ʵ���Ϊ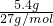 =0.2mol�����÷�Ӧ�жϽ����������������������ɣ�
=0.2mol�����÷�Ӧ�жϽ����������������������ɣ�
���200.0mL?2.0mol?L-1��ij��Һ�����ʵ����ʵ���Ϊ0.2L��2.0mol?L-1=0.4mol��Al�����ʵ���Ϊ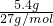 =0.2mol��
=0.2mol��
A����Al��HNO3��Һ�������������������⣬��A����
B����2Al+2OH-+2H2O�T2AlO2-+3H2����0.2molAl��0.4molBa��OH��2��Һ��Ӧʱ�����������B����
C����2Al+6H+�T2Al3++3H2����0.2molAl��0.4molH2SO4��Һ�������������C����
D����2Al+6H+�T2Al3++3H2����0.2molAl��0.4molHCl��Һ��Al��������D��ȷ��
��ѡD��
���������⿼�����Ļ�ѧ���ʣ���ȷ���������Ļ�ѧ��Ӧ�ǽ��Ĺؼ�����ע�����������жϹ������⼴�ɽ��
�����Ѷȣ�һ��