微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于物质的用途,不正确的是
A.小苏打可用于治疗胃酸过多
B.Cl2可与石灰乳反应制取漂白粉
C.镁铝合金可用作制造飞机的材料
D.高纯硅用来制造光导纤维
参考答案:D
本题解析:分析:A、小苏打是碳酸氢钠和胃酸中的盐酸反应;
B、氯气和石灰乳氢氧化钙反应是工业制备漂白粉的制备方法;
C、镁铝合金质量轻硬度大;要制造飞机,就是在飞机机身体积不变的情况下,飞机的机身越轻越有利于飞机的飞行;
D、高纯硅制备太阳能电池板,光导纤维是二氧化硅;
解答:A、小苏打是碳酸氢钠和胃酸中的盐酸反应,碱性不强,可用于治疗胃酸过多,故A正确;
B、氯气和石灰乳氢氧化钙反应是工业制备漂白粉,Cl2可与石灰乳反应制取漂白粉,故B正确;
C、镁铝合金质量轻硬度大,镁铝合金可用作制造飞机的材料,故C正确;
D、高纯硅制备太阳能电池板,光导纤维是二氧化硅,故D错误;
故选D.
点评:本题考查了物质性质和用途的分析判断,掌握基础,理解性质应用是解题关键,题目较简单.
本题难度:困难
2、选择题 将Na2CO3?10H2O与NaHCO3的混合物m?g溶解于水,配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,若将溶液蒸干并加热至质量不变,可得固体的质量是
A.1.86g
B.2.55g
C.2.12g
D.无法确定
参考答案:C
本题解析:分析:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,最后得到的固体为Na2CO3,根据Na元素守恒可计算Na2CO3的物质的量,进而计算Na2CO3的质量.
解答:将Na2CO3?10H2O与NaHCO3的混合物mg溶解于水,将溶液蒸干并加热至质量不变,
NaHCO3加热分解生成Na2CO3,最后得到的固体为Na2CO3,
配制成100mL溶液,测知溶液中Na+的质量m(Na+)=0.92g,
则n(Na+)=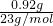 =0.04mol,
=0.04mol,
n(Na2CO3)= n(Na+)=0.04mol×
n(Na+)=0.04mol× =0.02mol,
=0.02mol,
m(Na2CO3)=0.02mol×106g/mol=2.12g,
故选C.
点评:本题考查混合物的计算,题目难度不大,本题注意加热后固体的成分的判断,根据Na元素守恒计算.
本题难度:一般
3、选择题 下列离子方程式书写正确的是
A.FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl-
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.FeS固体放入稀硝酸溶液中:FeS+2H+=Fe2++H2S↑
D.AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O
参考答案:B
本题解析:分析:A、离子方程式中电荷不守恒;
B、酸式盐和碱反应,量少的全部反应,离子方程式中符合化学式组成比;
C、硝酸具有强氧化性能氧化硫化亚铁;
D、氢氧化铝不溶于氨水弱酸;
解答:A、FeCl2溶液中通入Cl2:2Fe2++Cl2=2Fe3++2Cl-,故A错误;
B、澄清石灰水与少量小苏打溶液混合,反应的离子方程式为:Ca2++OH-+HCO3-=CaCO3↓+H2O,故B正确
C、FeS固体放入稀硝酸溶液中,稀硝酸具有强氧化性,能氧化硫化亚铁为三价铁离子和硫酸,故C错误;
D、AlCl3溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;故D错误;
故选B.
点评:本题考查了离子方程式的正误判断和书写方法,主要考查氧化还原反应的电子守恒,关键是稀硝酸的强氧化性,氢氧化铝不溶于弱碱.
本题难度:一般
4、选择题 向0.1mol?L-1NaOH溶液中通入过量的CO2后,溶液中存在的主要离子是下列的
A.Na+和CO32-
B.Na+和HCO3-
C.HCO3-和CO32-
D.Na+和OH-
参考答案:B
本题解析:分析:先写出反应方程式,根据方程式中的生成物判断存在的主要离子.
解答:氢氧化钠和过量的二氧化碳反应生成碳酸氢钠NaOH+CO2=NaHCO3,碳酸氢钠是强碱弱酸酸式盐,在水溶液里电离出自由移动的钠离子和碳酸氢根离子,碳酸氢根能水解也能电离,但都比较微弱,所以溶液中存在的主要离子是钠离子和碳酸氢根离子,故选B.
点评:知道氢氧化钠和过量的二氧化碳反应产物及碳酸氢钠的电离方程式是解本题的关键;碳酸氢根离子既能电离又能水解,但都比较微弱,其水解程度大于电离程度,所以碳酸氢钠水溶液呈碱性.
本题难度:简单
5、选择题 将1.62g淀粉在一定条件下水解,反应一段时间后,向容器中加入足量的银氨溶液,结果析出0.108g银,则淀粉的水解率为?
A.8%
B.10%
C.5%
D.无法计算
参考答案:C
本题解析:试题分析:银的物质的量是0.108g÷108g/mol=0.001mol,所以根据反应的化学方程式CH2OH(CHOH)4CHO+2Ag(NH3)2OH CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O可知,葡萄糖的物质的量是0.0005mol。根据淀粉水解的方程式
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O可知,葡萄糖的物质的量是0.0005mol。根据淀粉水解的方程式
 可知,淀粉的水解率是
可知,淀粉的水解率是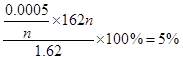 ,答案选C。
,答案选C。
考点:考查淀粉水解、银镜反应的有关计算
点评:该题是常规性试题的考查,难度不大。主要是有利于培养学生的规范答题能力,特别是学生的逻辑推理能力。该题的关键是熟练掌握有关的反应原理,然后灵活运用即可。
本题难度:一般