微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (本小题满分9分)
(1)把6 mol A气体和5 mol B气体混合放入4 L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L・min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
2C(g)+xD(g),经5min达到平衡,此时生成2 mol C,测得D的平均反应速率为0.15 mol/(L・min),则平衡时A的物质的量浓度是____________;B的转化率是__________;x的值是___________。
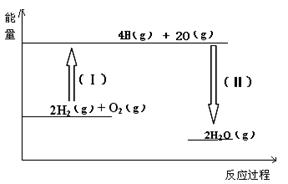
(2)反应2H2(g) + O2(g)= 2H2O(g)的能量变化如图所示。已知拆开1molH2、1molO2和1molH-O中的化学键分别需要消耗436KJ、496KJ和463KJ能量,则该反应??(填“吸收” 或“放出”)??KJ热量。
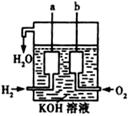
(3)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如右图所示:
a、b两个电极均由多孔的碳块组成。写出a极的电极反应式:?。
(4)工业上用电解饱和食盐水的方法制取金属氯气,反应中能量的转化形式是?;氯气在?极上产生,反应后溶液的pH?。(填“增大”或“减小”)。
参考答案:(9分,每空各1分)(1)0.75mol/L? 20%? 3?(2)放出? 484
(3)H2 +2OH--2e-=2H2O?(4)电能转化为化学能?阳?增大
本题解析:(1)D的平均反应速率为0.15 mol/(L・min),所以生成物B平衡时物质的量是0.15 mol/(L・min)×5min×4L=3mol,因为物质的量的变化量就是相应的化学计量数之比,所以x=3.消耗AB的物质的量分别是3mol和1mol,因此平衡时A的浓度是(6mol-3mol)÷4L=0.75mol/L,B的转化率是1÷5×100%=20%。
(2)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应放出的能量是2×2×463KJ-2×436KJ-496KJ=484KJ。
(3)a极通入的是空气,所以是负极,又因为电解质溶液是氢氧化钾,所以负极反应式为H2 +2OH--2e-=2H2O 。
(4)电解是把电能转化为化学能的装置。电解池中阴离子在阳极放电,所以阳极产生氯气。阴极是氢离子放电,产生氢气。所以溶液中产生氢氧化钠,显碱性,pH增大。
本题难度:一般
2、选择题 在定温、定容条件下,能标志H2(g)+I2?(g)?

?2HI?(g)达平衡的是( )
A.单位时间内消耗amolH2,同时消耗2amolHI
B.容器内的总压强不随时间变化
C.容器内H2、I2不再减少,HI不再增加
D.单位时间内每生成amolHI,同时a个HI分子分解
参考答案:A、单位时间内消耗amolH2同时生成2amolHI,且同时又消耗2amolHI,所以碘化氢的正逆反应速率相等,达到平衡状态,故A正确;
B、该反应是反应前后气体体积不变的化学反应,所以无论反应是否达到平衡状态混合气体的压强始终恒定不变,故B错误;
C、反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,所以容器内H2、I2不再减少,HI不再增加,该反应达到平衡状态,故C正确;
D、单位时间内每生成amolHI,同时a个HI分子分解,反应方向相反但速率不相等,故D错误;
故选AC.
本题解析:
本题难度:简单
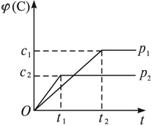
3、选择题 在一定温度下的可逆反应:mA(g)+nB(g)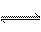 pC(g)+qD(g),生成物C的体积分数与压强p1和p2,时间t1和t2的关系如下图所示,则下列关系正确的是(? )
pC(g)+qD(g),生成物C的体积分数与压强p1和p2,时间t1和t2的关系如下图所示,则下列关系正确的是(? )
A.p1>p2
B.p1<p2
C.m+n>p+q
D.m+n<p+q
参考答案:BD
本题解析:由图象可知:本题是起始反应物为A、B,生成物为C、D的可逆反应(注意起点),从反应开始达到平衡的反应过程。图象显示,压强为p1时,在t2达到平衡,生成物C的体积分数为c1;压强为p2时,在t1达到平衡,生成物C的体积分数为c2。从横坐标看,t2>t1,说明p2时化学反应速率快,先达到平衡,所以压强p2>p1;从纵坐标看,c1>c2,说明加压将使平衡向逆反应方程移动,即p+q>m+n。
本题难度:一般
4、填空题 (15分)
在溶液中,反映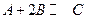 分别在三种不同实验条件下进行,它们的起始浓度均为
分别在三种不同实验条件下进行,它们的起始浓度均为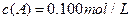 、
、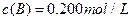 及
及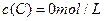 。反映物A的浓度随时间的变化如下图所示。
。反映物A的浓度随时间的变化如下图所示。
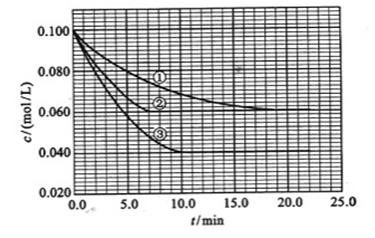

请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②_____________;
③______________;
(2)实验②平衡时B的转化率为_________;实验③平衡时C的浓度为__________;
(3)该反应的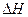 >0,判断其理由是________________;
>0,判断其理由是________________;
(4)该反应进行到4.0min时的平均反应速度率:
实验②: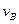 =___________;
=___________;
实验③: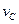 =_______________。
=_______________。
参考答案:
(1)加催化剂,达到平衡的时间缩短,平衡时A的浓度未变
温度升高,达到平衡的时间缩短,平衡时A的浓度减小。
(2)4.0%?;0.06mol/l
(3)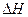 >0;温度升高,平衡向正反应方向移动,故该反应是吸热反应。
>0;温度升高,平衡向正反应方向移动,故该反应是吸热反应。
(3)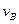 =0.014mol・L-1・S-1?;
=0.014mol・L-1・S-1?;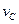 =0.009mol・L-1・S-1
=0.009mol・L-1・S-1
本题解析:略
本题难度:简单
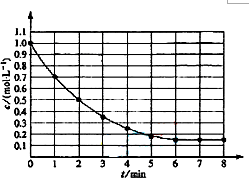
5、选择题 右图表示反应X(g)  4Y g)+Z g);△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是(?)
4Y g)+Z g);△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是(?)
A.第6min后,反应就终止了
B.若降低温度,v正和v逆将以同样倍数减小
C.X的平衡分解率为85%
D.若升高温度,.X的平衡分解率为85%
参考答案:C
本题解析:A 错第6min后,反应达到了平衡,不是反应终止
B 错降低温度,反应速率降低,但平衡右移,v正降低比v逆降低慢
C 对达到平衡时,A的浓度变化量为1.0-0.15=0.85,那么.X的平衡分解率为85%
D 错升温,平衡左移,X的转化率减小,.X的平衡分解率小于85%
本题难度:简单