微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有Fe2+、NO-3、Fe3+、NH+4、H+和H2O六种粒子,分别属于同一个氧化还原反应中的反应物和生成物。下列叙述正确的是
A.反应中NH+4被氧化
B.氧化剂与还原剂的物质的量之比为8:1
C.若有10molH+参加反应,则生成的水的物质的量为5mol
D.生成物中加入KSCN溶液后变红色
参考答案:D
本题解析:通过观察可知,亚铁离子在酸性条件下被硝酸根离子氧化为铁离子,铁离子遇KSCN溶液变为红色。反应的离子方程式为,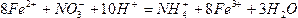 。
。
本题难度:一般
2、选择题 用NA表示阿伏伽德罗常数的数值,下列说法正确的是
A.1L 1mol・L-1的NH4NO3溶液中氮原子数小于2 NA
B.常温常压下
C.11.2 g乙烯中含有共用电子对数目为2.4 NA
D.在O2参加的反应中
E.1molO2作氧化剂时得到的电子数一定是4 NA
F.标准状况下
G.22.4 L CCl4中所含有的分子数为NA
参考答案:B
本题解析:
A不正确,因为水解反应很微弱,不能放出氨气,氮原子数等于2 NA。
B正确11.2 g乙烯是11.2g÷28g/mol=0.4mol,所以根据乙烯的结构式可知,含有共用电子对0.4mol×6=2.4mol。
C不正确,例如和钠反应生成过氧化钠中,1mol氧气得到2mol电子。
D不正确,标准状况下,四氯化碳不是气体,不能用于气体摩尔体积,答案选B。
本题难度:困难
3、选择题 下列表示方法中,错误的是
A.1mol氮
B.1molO
C.1molNa+
D.1molH2CO3
参考答案:A
本题解析:在用摩尔表示微粒时,一般用微粒的化学式表示,而不用汉字,所以选项A是错误的,其余都是正确的,答案选A。
本题难度:一般
4、选择题 某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
参考答案:A
本题解析:溶液显酸性,所以选项C不正确;醋酸是弱酸,所以在选项A中醋酸是过量的,A正确;B中二者恰好反应,生成的醋酸钠水解溶液显碱性,B不正确;D不正确,根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+)可知,c(CH3COO-)一定小于c(Na+)、c(NH4+)之和,答案选A。
考点:考查溶液中离子浓度大小比较
点评:在判断溶液中离子浓度大小比较时,必须根据几个守恒关系,即电荷守恒、物料守恒和质子守恒等。
本题难度:简单
5、选择题 下列物质中加入金属钠不产生氢气的是
A.乙醇
B.乙酸
C.水
D.苯
参考答案:D
本题解析:
本题难度:一般