微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 硫化氢(H2S)分子中,两个H-S键的夹角接近90°,说明H2S分子的空间构型为___________;二氧化碳(CO2)分子中,两个C=O键的夹角是180°,说明CO2分子的空间构型为___________;甲烷(CH4)分子中,两个相邻C-H键的夹角是109°28′,说明CH4分子的空间构型为___________。
参考答案:折线型;直线型;正四面体型
本题解析:
本题难度:一般
2、填空题 分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体。顺铂的结构式为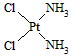 ,具有抗癌作用;反铂的结构式为
,具有抗癌作用;反铂的结构式为 ,无抗癌作用。
,无抗癌作用。
(1)C、N、O三种元素的电负性由大到小的顺序是___________________。
(2)顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由:____________________。
(3)金属铂的原子堆积方式为与铜型(面心立方堆积),一个金属铂的晶胞中含有_______个铂原子。
(4)NH3还能与很多化合物通过配位键发生相互作用。例如:科学家潜心研究的一种可作储氢材料的化合物X是NH3与第二周期另一种元素的氢化物相互作用的产物,X是乙烷的等电子体;加热化合物X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体。
① 化合物X的结构式为____________(必须标明配位键)。
② 化合物X、Y分子中,N元素分别发生了________________杂化。
参考答案:(1)O>N>C?
(2)顺铂易溶于水,因为它是极性分子,易溶于极性溶剂
(3)4
(4)①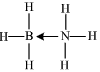 ;②sp3和sp2
;②sp3和sp2
本题解析:
本题难度:一般
3、填空题 (8分)有下列九种晶体,完成下列各小题。
①金刚石 ②C60? ③锌④晶体氖? ⑤氯化铵 ⑥金刚砂 ⑦冰醋酸? ⑧干冰 ? ⑨氧化钠?
(1)属于分子晶体的是________,属于原子晶体的是________,属于离子晶体的是________。
(2)属于电解质的是________。
(3)直接由原子构成的晶体是________。
(4)含有极性共价键的晶体是_______?_。
(5)晶体中有氢键的是________________,受热熔化需克服共价键的是________。
参考答案:(1)②④⑦⑧,①⑥,⑤⑨?(2)⑤⑦⑨?(3)①④⑥?(4)⑤⑥⑦⑧?(5)⑦,①⑥
本题解析:依据构成晶体的微粒和微粒间的相互作用,可以确定分子晶体为C60,晶体氖,冰醋酸,干冰;原子晶体为金刚石,金刚砂;离子晶体为氯化铵,氧化钠。根据水溶液或熔融状态下能否导电可以确定电解质是氯化铵,冰醋酸,氧化钠;直接由原子构成的晶体除了原子晶体外还有稀有气体;含有极性共价键的晶体为氯化铵,金刚砂,冰醋酸,干冰;晶体中有氢键的为冰醋酸,受热熔化需要克服共价键的是原子晶体。
点评:这类习题综合性强,主要考查对物质进行晶体分类,考试中的热点题型。
本题难度:一般
4、选择题 如图所示是a、b两种不同物质的熔化曲线,下列说法正确的是
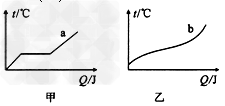
[? ]
A.a是晶体
B.a是非晶体
C.b是晶体
D.b是非晶体
参考答案:AD
本题解析:
本题难度:简单
5、选择题 下列说法正确的是
A.碳酸氢根离子的电离方程式: HCO3-+H2O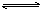 H3O++ CO32-
H3O++ CO32-
B.从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
C.因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
D.NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着6个Cs+
参考答案:A
本题解析:本题考查电离平衡、元素周期律及晶体结构知识;碳酸氢根,是弱酸酸式根,存在电离平衡,A正确;卤族元素从上到下,氢卤酸的酸性依次增强,B错误;非金属性强弱的判断,依据最高价氧化物对应水化物酸性强弱,HClO不是最高价含氧酸,不能做为判断的依据,C错误;CsCl晶体中每个Cl-同时吸引着8个Cs+,D错误。
本题难度:一般