��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������X��Һ���ֱ����ʢ��10 mL 2 mol��L-1 HCl�ձ��У���ˮϡ����50 mL��X��HCl���з�Ӧ,���з�Ӧ����������(? )
A��20 mL 3 mol��L-1 X����Һ
B��20 mL 2 mol��L-1 X����Һ
C��10 mL 4 mol��L-1 X����Һ
D��10 mL 2 mol��L-1 X����Һ
�ο��𰸣�A
���������������������Է�Ӧ���ʵ�Ӱ�졣����Ӧ���Ũ�ȣ��������¶ȣ�������Ӧ��ĽӴ��������ʹ�ô����ȶ���ʹ��Ӧ���ʼӿ졣�������⣬������������ͬʱ��ѡ��A��X��Ũ����ߣ����Է�Ӧ�������ѡA��
�����Ѷȣ���
2��ѡ���� ��֪��2X+Y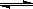 2Z����Ӧ�Цأ�Z�����ʵ������������¶�T�ı仯����ͼ��ʾ�������ж���ȷ����
2Z����Ӧ�Цأ�Z�����ʵ������������¶�T�ı仯����ͼ��ʾ�������ж���ȷ����
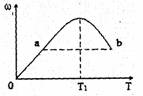
A��T1ʱ��v��>v��
B������Ӧ�ġ�H��0
C��a��b����ķ�Ӧ����va=vb
D��T��T1ʱ���������ԭ����ƽ�����������ƶ�
�ο��𰸣�B
�����������ͼ���֪����ӦΪ���ȷ�Ӧ��T1ʱΪƽ��״̬A��T1ʱv����v�棬����C��b���¶ȸߣ������ʴ�a��b����ķ�Ӧ����va��vb ������ D��T��T1ʱ���������ԭ���Ƿ�Ӧ��û�дﵽƽ�⣬����
�����Ѷȣ�һ��
3��ѡ���� һ������ϡ���������п�۷�Ӧʱ��Ϊ�˼�����Ӧ�����ֲ�Ӱ������H2���������ɲ�ȡ�Ĵ�ʩ��
[? ]
A����������ϡNaOH��Һ?
B����������CH3COONa����
C����������CuSO4����?
D������
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ������������п��a��b�ֱ���뵽����������ͬ�Ĺ�����ϡ�����У�ͬʱ��a�м���������CuSO4��Һ�����и�ͼΪ����H2�����V��L����ʱ��t��min���Ĺ�ϵ��������ȷ���ǣ�?��
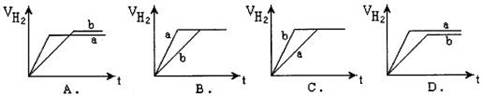
�ο��𰸣�A
�����������a�м���������CuSO4��Һ,����п������ͭ��Ӧ�����ɵ��������٣����ɵ�ͭ������п�ı��棬����ԭ��أ��ӿ췴Ӧ���ʣ���ѡA��
�����Ѷȣ�һ��
5��ѡ���� ������Fe����һ���������ᷴӦ��Ϊ�˼�����Ӧ���ʣ����ֲ�Ӱ�����������������Ӧ�������������е�
A��NaNO3��Һ
B��NaCl����
C��Na2SO4��Һ
D��CuSO4��ĩ
�ο��𰸣�C
���������
���������ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ������������������Դ������
�⣺���ݷ����ķ�ӦΪFe+2H+�TFe2++H2�������С�����ӵ�Ũ�ȶ����ı������ӵ����ʵ����������������Ӧ���ʣ����ֲ�Ӱ�����������������
A������NaNO3��Һ��Fe����������ӡ������ӷ���������ԭ��Ӧ����NO������������������A����
B������NaCl���壬�Է�Ӧ��Ӱ�죬���������Ӧ���ʣ���B����
C������Na2SO4��Һ�������Ʋ����뷴Ӧ����Һ�������������ӵ�Ũ�ȼ�С���������ӵ����ʵ���û�б仯����Ӧ���ʼ��������ֲ�Ӱ�������������������C��ȷ��
D������CuSO4������Fe��Cu������ԭ��أ��ӿ췴Ӧ���ʣ���D����
��ѡC��
�����Ѷȣ�һ��