��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣�������Ԫ��A��B��C��D�У�0.5mol AԪ�ص����ӵõ�6.02��1023�����ӱ���ԭΪ����ԭ�ӣ�0.4g A��������ǡ����100ml 0.2mol/L��������ȫ��Ӧ��Aԭ�Ӻ���������Ŀ��������Ŀ��ȣ�BԪ��ԭ�Ӻ�������������Ŀ�ȵ�һ���1����C�D��AԪ�ص����Ӷ�1�����Ӳ㣬DԪ�ص�ԭ�Ӻ���ڶ���ȵ�һ���2�����ӡ��ش��������⣺
(1)AԪ�ص�������_______��
��2��C�D�Ľṹʾ��ͼΪ?��DԪ�������ڱ��е�λ����__________��
��3��Ԫ��D����̬�⻯��ĵ���ʽΪ____������ӵĽṹ�ص��Ǿ���_____�ṹ����һ�������¸��⻯����뵥��C����ȡ����Ӧ�����������ʵ����ĸ��⻯���뵥��C��ϣ���һ�������³�ַ�Ӧ�������������ʵ���������_______���û�ѧʽ��д����
��4����ҵ��ұ������A�Ļ�ѧ����ʽΪ_____________________________________��
��5����ҵ�ϳ��õ���Bұ�����۵Ľ�����д���������͵���B�ڸ����·�Ӧ�Ļ�ѧ����ʽ_______������Ӧ����0.25mol�������μӷ�Ӧ��Ӧ��ת�Ƶ��ӵĸ���Ϊ__________��
��6����������A��B�õ������Ӳ��뵽����������Һ�п������ԭ��أ���������
����_______���û�ѧʽ��д���������缫��Ӧ��___________________________________��
�ο��𰸣�(1)þ? (2) 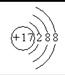 ���ڶ����ڡ���A? (3)
���ڶ����ڡ���A? (3)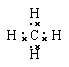 ����������? HCl?
����������? HCl?
(4) MgCl2(����) Mg��Cl2��?��5��Fe2O3��2Al
Mg��Cl2��?��5��Fe2O3��2Al Al2O3��2Fe? 9.03��1023
Al2O3��2Fe? 9.03��1023
��6��Mg? 2Al��6e����8OH��=2AlO2����4H2O
�������������Ԫ�ص����ʺ������ڱ��е�λ�ÿ�֪��B����Ԫ�أ�D��̼Ԫ�ء�0.5mol AԪ�ص����ӵõ�6.02��1023�����ӱ���ԭΪ����ԭ�ӣ�˵��A������ǣ�2�ۡ�100ml 0.2mol/L��������0.02mol����������������ʵ�����0.01mol���Ҵ���Է���������40����A����������24. Aԭ�Ӻ���������Ŀ��������Ŀ��ȣ�����A��þ����C����Ԫ�ء�
��3�������Ǿ�����������ṹ���ӣ������ʽΪ �������к���4����ԭ�ӣ������������к����������Ȼ��⡣
�������к���4����ԭ�ӣ������������к����������Ȼ��⡣
��4��þ�ǻ��õĽ�����ͨ��������ڵ��Ȼ�þ����þ������ʽΪMgCl2(����)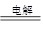 Mg��Cl2����
Mg��Cl2����
��5�����ǻ��õĽ������������ȷ�Ӧ�ķ���ʽΪFe2O3��2Al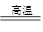 Al2O3��2Fe�������������Ļ��ϼ��ǣ�3�۵ģ�����0.25mol�������μӷ�Ӧת�Ƶĵ���Ϊ0.25mol��3��2��1.5mol���������Ϊ1.5mol��6.02��1023��9.03��1023��
Al2O3��2Fe�������������Ļ��ϼ��ǣ�3�۵ģ�����0.25mol�������μӷ�Ӧת�Ƶĵ���Ϊ0.25mol��3��2��1.5mol���������Ϊ1.5mol��6.02��1023��9.03��1023��
��6��������������������Һ��Ӧ������������������þ��������������ӦʽΪ2Al��6e����8OH��=2AlO2����4H2O��
�����Ѷȣ�һ��
2������� (6��)? A��B��C����Ԫ�ض��Ƕ�����Ԫ�ء�����AԪ�ص����ʣ�����ɫ����������ʱ������ɫ���棻B2����Ȼ������������壬 AԪ����CԪ��λ��ͬһ���ڣ�B2��C2��ȼ�ղ�����ɫ���棬�ҿ��γɹ��ۻ�����������������ش�
�� д��A��B��Ԫ�ط��ţ�A?��B?��
�� д��CԪ������������Ӧˮ����Ļ�ѧʽ?��
�ο��𰸣���6�֣�
��? Na ,? H��? HClO4
�����������ɫ��ӦΪ��ɫ�������бغ���NaԪ�أ�B2����Ȼ������������壬��ΪH2��ȼ��ʱ������ɫ�����ΪH2��CL2��Ӧ��
CԪ��ΪCLԪ�أ������Ϊ+7�ۣ���Ӧ�������ﻯѧʽΪHClO4
�����Ѷȣ���
3��ѡ���� X��Y��Z��W��R���ֶ�����Ԫ����Ԫ�����ڱ��е�λ����ͼ��ʾ�������й�˵��һ����ȷ����
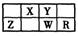
A���ǽ����Ե�ǿ��˳��Y>W>R
B��X��Y����̬�⻯����ȶ��ԣ�X>Y
C��ԭ�Ӱ뾶�Ĵ�С˳��Z>W>Y
D ��W��R������������Ӧˮ��������ԣ�W>R
��W��R������������Ӧˮ��������ԣ�W>R
�ο��𰸣�C
�����������
�����Ѷȣ���
4������� ��1����Ҫ����գ��縺������Ԫ�ط��� ______����һ����������Ԫ�ػ�̬ԭ�Ӻ�������Ų�ʽ_________����������ԭ�Ӱ뾶��С��Ԫ�صļ۵����Ų�ʽ______��
��2�������������У���N2����H2O����NaOH����MgCl2����C2H4����Na2O2���������գ�
����ֻ���зǼ��Լ�����?��ֻ���м��Լ�����?��ֻ�������Ӽ�����?���Ⱥ��зǼ��Լ��ֺ��м��Լ�����?�����зǼ��Լ������ӻ�������?��
��3��N��N�ļ���Ϊ942kJ��mol-1��N��N�����ļ���Ϊ247kJ��mol-1��ͨ������˵��N2�е�?�����ȶ�����ҡ��С�����
�ο��𰸣���9�֣���1��F? 1s2? 3s23p5?��2���٣��ڣ��ܣ��ݣ���?��3���� ����1�֣�
�����������1���ǽ�����Խǿ���縺��Խ�����Ե縺��������F��He����������ֻ��2�����ȶ���ǿ����һ������������̬ԭ�Ӻ�������Ų�ʽ��1s2��ͬ�����������ң�ԭ�Ӱ뾶��С�����Ե�������ԭ�Ӱ뾶��С��Ԫ������Ԫ�أ���۵����Ų�ʽ��3s23p5��
��2��һ����õĽ����ͻ��õķǽ��������γ����Ӽ����ǽ���Ԫ�ص�ԭ�Ӽ������γɹ��ۼ����������ͬһ�ַǽ�����ԭ��֮���γɹ��ۼ����ǷǼ��Լ����ɲ�ͬ�ַǽ�����ԭ��֮���γɹ��ۼ����Ǽ��Լ�������ֻ���зǼ��Լ����ǵ�����ֻ���м��Լ�����ˮ��ֻ�������Ӽ������Ȼ�þ���Ⱥ��зǼ��Լ��ֺ��м��Լ�������ϩ�����зǼ��Լ������ӻ������ǹ������ƣ����������Ǻ������Ӽ��ͼ��Լ������ӻ����
��3�������е���������1���ļ���2���м����ɵģ����Ը���N��N�ļ���Ϊ942kJ��mol-1��N��N�����ļ���Ϊ247kJ��mol-1��֪���м������ǣ�942kJ/mol��247kJ/mol����2��347.5 kJ/mol��247kJ/mol�����Ԧм��ȶ���
�����������Ǹ߿��еij������ͺͿ��㣬�����е��Ѷ�����Ŀ��顣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ������Ҫ�ǿ���ѧ������������ʽṹ֪ʶ���ʵ�����������������������ѧ����������������Ӧ�����������ѧ����ѧ��������
�����Ѷȣ�һ��
5������� ��8�֣�ԭ�ӽṹ��Ԫ�����ڱ�������������ϵ��������ѧԭ�ӽṹ������֪ʶ����ش��������⣺
��1�����У�n-1��d10ns2���ӹ��͵�Ԫ��λ�����ڱ���?�塣
��2������Ϊ��21���͵Ľ��������ѣ�Ti��Ԫ��ԭ�ӵļ۵����Ų�ʽΪ��?��
��3��д����Ԫ��ԭ�ӵĺ�������Ų�ʽ?��
��4��д��3p�������2��δ�ɶԵ��ӵ�Ԫ�صķ��ţ�?��
�ο��𰸣�����8�֣�ÿ��2�֣���1����B?��2��3d24s2? (3)1s22s22p63s23p1? (4)? Si? S
�����������1�����ݼ۵��ӵ��Ų�ʽ��֪����Ԫ��Ӧ��λ�ڵڢ�B��
��2���ѵ�ԭ��������22�����Ը��ݹ���ԭ����֪����Ԫ��ԭ�ӵļ۵����Ų�ʽ��
1s22s22p63s23p13d24s2��
��3�����ݹ���ԭ����֪��3p�������2��δ�ɶԵ��ӵ�Ԫ����Si��S��
�����Ѷȣ�һ��