��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����Լռ����������71%������ʮ�־�Ŀ���DZ����ijУ�о���ѧϰС��ͬѧ�Ծ���������������Ũ����ˮ����Ҫ��NaCl��MgSO4�������о���
��1��ʵ��ʱ����������ƽ����500mL0.20mol/LNaOH��Һ�������������NaOH��������
��2��ȡ��������������Ũ����ˮ100mL������200mL0.20mol/LNaOH��Һ��ǡ�ð����е�Mg2+��ȫ��������Ũ����ˮ��Mg2+�����ʵ���Ũ��Ϊ���٣�
��3���о�С��ͬѧ������������ȫת��Ϊ��ˮMgCl2����������״̬�½��е�⣬�ɵñ�״����Cl2��������
�ο��𰸣���1���������Ƶ����ʵ���n��NaOH��=C��NaOH����V=0.20mol/L��0.5L=0.10mol��
����NaOH������m��NaOH��=n��NaOH��?M��NaOH���T0.10mol��40g/mol=4.0g��
�𣺹���NaOH������Ϊ4.0g��?
��2����������þ�����ʵ���Ϊx��
? MgCl2 +2NaOH�TMg��OH��2��+2NaCl
? 1? 2
?x? ?0.20L��0.20mol/L
? ?1x=20.20L��0.20mol/L
? x=0.02mol
?����c��Mg2+��=0.02mol?0.1L=0.2mol/L?
��Ũ����ˮ��Mg2+�����ʵ���Ũ��Ϊ0.2mol/L��
��3�������������ʵ���Ϊy��
? MgCl2�����ڣ�??ͨ��?.? Mg+Cl2��
? ?1? 1
? 0.02mol? y
? 1?0.02mol=1y
? y=0.02mol
? V��Cl2��=0.02mol/L��0.1L��22.4L/mol=0.448L?
�𣺿ɵñ�״��������0.448L��
���������
�����Ѷȣ�һ��
2��ѡ���� �±��ж����ӷ���ʽ��д��������ȷ����
[? ]
��ѧ��Ӧ�����ӷ���ʽ
����
A.
��ͭм���뺬Fe3+��Һ�У�Fe3++Cu=Fe2++Cu2+
��ȷ
B.
Na2O2��H2O��Ӧ��Na2O2+H2O=2Na++2OH-+O2��
������Ԫ�ز��غ�
C.
NaOH��Һ����������Ӧ��Al2O3+2OH-=2AlO2-+H2O
������Ӧ����Al(OH)3
D.
��Fe(OH)2�м�������ϡ���Fe(OH)2+2H+=Fe2++2H2O
��ȷ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��д��ȷ����
[? ]
A��ʯ������Na2CO3��Һ��ϣ�Ca2++CO32-��CaCO3��
B��NH4HSO3��Һ��������NaOH��Һ��ϼ��ȣ�NH4++HSO3-+2OH- NH3��+SO32-+2H2O
NH3��+SO32-+2H2O
C������������KIO3��Һ��KI��Һ������Ӧ����I2��IO3-+5I-+3H2O��3I2+6OH-
D������ͭ���ռӦ��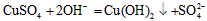
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ѡ���� ���и���Ӧ�����ӷ���ʽ��,��д��ȷ����(? )
A�� NaOH��Һ��HCl��Ӧ: H+ + OH- = H2O
B�� FeCl3��Fe��Ӧ: Fe3+ +Fe = 2Fe2+
C�����������������Ӧ: H+ + SO42- + Ba2+ +OH- = H2O + BaSO4��
D������ͭ��ϡ���ᷴӦ: CuO + 2H+ = Cu2+ + H2O
�ο��𰸣�AD
���������A ��
B �� ��ɲ��غ�
C �� 2H+ + SO42- + Ba2+ +2OH- = 2H2O + BaSO4��
D ��
�����Ѷȣ�һ��
5��ѡ���� ����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��?
A��Fe3O4��������ϡHNO3��Fe3O4��8H+��Fe2����2Fe3��+ 4H2O
B��NH4HCO3��Һ������Ba(OH)2��Һ��ϣ�HCO3����Ba2����OH����BaCO3����H2O
C�������ʯ��ˮ��ͨ������CO2�� OH-��CO2�� HCO3��
D����0.2 mol��L-1��NH4Al(SO4)2��Һ��0.3 mol��L-1��Ba(OH)2��Һ�������ϣ�
2Al3����3SO42����3Ba2����6OH����2Al(OH)3����3BaSO4��
�ο��𰸣�D
���������A�ϡ������������ԣ���������������ͬʱ����NO���塣Ӧ��Ϊ��3Fe3O4��NO3-+28H+��9Fe3��+ NO+14H2O��A����
B�Ba(OH)2��Һ��������HCO3����笠����Ӷ��������������ӷ�Ӧ��B����
C�������̼����ʱӦ��������̼��ƣ�����ʱ��������ʽ�Ρ�C����
D�NH4Al(SO4)2��Һ��Ba(OH)2��Һ���ʵ���֮��Ϊ2:3�� 2mol Al3��ǡ��6mol OH����Ӧ��������������������NH4+�����������Ӳ��㲻�ܷ�Ӧ��3mol Ba2��ֻ������3mol SO42����SO42��û����ȫ�������ӷ�Ӧ��D�ԡ�
��ѡD
�����Ѷȣ�һ��