| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ܽᡶ�����Ļ�ѧ��Դ�����⼼�ɣ�2017�����°棩(ʮ)
�ο��𰸣�C ����������Ҵ���Ϊһ��ȼ�ϣ��ڷ�Ӧ��ʧȥ���ӣ��������������ȼ�ϵ�����Ҵ��ڸ����Ϸ�����Ӧ��A������ʧȥ���ӣ������ص��ߴ��ݵ������ϣ������Һ�е��������������ƶ������������ƶ�B����������������Ӧ��C��ȷ���Ҵ���̼ԭ�ӵĻ��ϼ��ǣ�2�ۣ����ڲ�����̼ԭ�ӵĻ��ϼ��ǣ�4�ۣ���1��̼ԭ��ʧȥ6�����ӣ�����1mol�Ҵ�ת��12mol���ӣ�����0.2mol�Ҵ�ת��2.4mol���ӣ����ص����������������������������ʵ���Ϊx������ת�Ƶ������غ㣬2x=2.4mol��x=1.2mol�����������������Ϊ1.2molx22.4L/mol=26.88L��D����ѡC. �����Ѷȣ����� 3������� ��14�֣��о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣 |
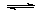 CH3OH(g)��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��2����ʾ���÷�Ӧ��H________0(�>����<��)��ʵ����������������250�桢
CH3OH(g)��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��2����ʾ���÷�Ӧ��H________0(�>����<��)��ʵ����������������250�桢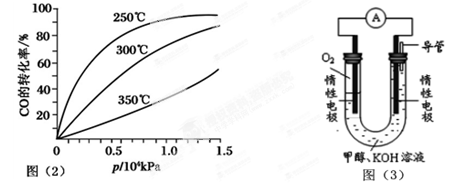
�ο��𰸣���1��-41.8��BD��1.8��
��2��������1.3��104kPa�£�CO��ת�����ѽϸߣ�������ѹǿCO��ת������߲��������ɱ����ӵò���ʧ��
��3�������� O2+2H2O+4e-=4OH-��
���������
��1�����ݸ�˹���ɣ����ڶ�������ʽ��д�����һ������ʽ��ӵã�2NO2(g)+2SO2(g)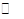 2SO3(g)+2NO(g)
2SO3(g)+2NO(g)
��H="-83.6" kJ?mol-1����NO2(g)+SO2(g) 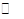 SO3(g)+NO(g) ��H="-41.8" kJ?mol-1��
SO3(g)+NO(g) ��H="-41.8" kJ?mol-1��
A������Ӧ�Ƿ�Ӧǰ���������������ķ�Ӧ������ϵ��ѹǿ���ֲ��䣬��A����˵����Ӧ�Ѵﵽƽ��״̬��
B�����ŷ�Ӧ�Ľ��У�NO2��Ũ�ȼ�С����ɫ��dz����B����˵����Ӧ�Ѵ�ƽ�⣻
C��SO3��NO�����������������1��1����C������Ϊƽ��״̬���ж����ݣ�
D������1molSO3Ϊ����Ӧ��ͬʱ����1mol NOΪ����Ӧ�������㻯ѧ������֮�ȣ�˵�����淴Ӧ������ȣ���D����Ϊƽ��״̬���ж����ݡ�
NO2(g)+SO2(g) 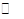 SO3(g)+NO(g)
SO3(g)+NO(g)
��ʼ���ʵ���� 2a a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� 2a-x a-x x x
ƽ��ʱNO2(g)��SO2(g)�������Ϊ5��1������������ʽ֪����2a-x������a-x����5��1����x��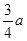 ����ƽ�ⳣ��K��
����ƽ�ⳣ��K��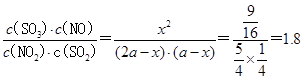 ��
��
��2����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ������淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H��0��ѹǿ�������ڼӿ췴Ӧ���ʣ�������ʹƽ�������ƶ�����ѹǿ������Ҫ�Ķ������豸��Ҫ��Ҳ�ߣ���ѡ��250�桢1.3��104kPa���ҵ���������Ϊ��250�桢ѹǿΪ1.3��104 kPaʱ��CO��ת�����ѽϴ�������ѹǿ��CO��ת���ʱ仯����û�б�Ҫ������ѹǿ��
��3���ٸ���ԭ��صĹ���ԭ�������������ƶ�������OH-���ƶ���
�ڵ������ҺΪ������Һ������������ӦΪ��O2+2H2O+4e-=4OH-��
����:�����˹���ɵ�Ӧ�ã��Ȼ�ѧ����ʽ����д����ѧƽ���־�жϣ�ԭ���ԭ��Ӧ��
����:���⿼���˸�˹���ɵ�Ӧ�ã��Ȼ�ѧ����ʽ����д����ѧƽ���־�жϣ�ԭ���ԭ����Ӧ�ã��Ѷ��еȡ����⽫Ԫ�ػ�����֪ʶ�������仯����ѧƽ���֪ʶ�����һ���ۺ��Խ�ǿ����Ҫϸϸ����������ͻ�ơ��״����ǣ�2����Ҫ�������ͼ�ó���ȷ���ۡ�
�����Ѷȣ�����
4��ѡ���� ﮷��������ص������ܶ�ԶԶ�����������ϵ�أ���ɱ��ͣ����ڴ����ƹ㣬
�ҶԻ�������Ⱦ������ܷ�ӦʽΪ��V2O5+xLi==LixV2O5������˵���У�����ȷ���ǣ�?��
A����������Ϊﮣ���������ΪV2O5
B�������ʱ����������������������ƶ�
C�������ĵ缫��ӦʽΪ��V2O5 + xLi++ xe��="=" LixV2O5
D�������ĵ缫��ӦʽΪ��xLi��xe��==xLi+
�ο��𰸣�A
������������ܷ�ӦV2O5+xLi==LixV2O5�Ļ��ϼ۸ı��֪������ߣ�ʧ���ӣ�Ϊ�������ϣ�xLi��xe��==xLi+����VԪ�صĻ��ϼ۽��ͣ�V2O5�õ��ӣ�Ϊ�������ϣ�V2O5 + xLi++ xe��="=" LixV2O5
�ʴ�ΪA
�����Ѷȣ���
5��ѡ���� �ɸ��ʼDZ����Թ���ļ״�ȼ�ϵ���Ѿ���������ṹʾ��ͼ���¡��״��ڴ����������ṩ����
��H+���͵��ӣ����Ӿ����·�����Ӿ��ڵ�·������һ�缫����������Ӧ������ܷ�ӦΪ��
2CH3OH+3O2=2CO2+4H2O������˵������ȷ����
[? ]
A���ҵ缫Ϊ���������b��ͨ��������ǿ���
B����缫Ϊ��ظ�����a��ͨ��������ǿ���
C��������ӦʽΪ��CH3OH+H2O��6e-=CO2+6H+
D��������ӦʽΪ��O2+4H++4e-=2H2O
�ο��𰸣�B
���������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ�ر�֪ʶ�㡶����������.. | |
| �����Ŀ |