��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��9�֣���ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱM��N�����缫�������������٣���ش��������⣺
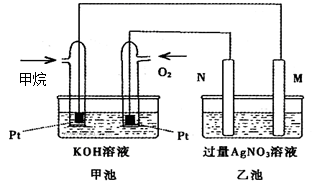
(1)M�缫�IJ�����?��N�ĵ缫�缫��ӦʽΪ��?���ҳص��ܷ�Ӧʽ��?��ͨ�����IJ��缫�Ϸ����ĵ缫��ӦʽΪ?__________________________?��
(2)�ڴ˹����У��ҳ���ijһ�缫����������4.32gʱ���׳�����������������Ϊ??L����״���£�������ʱ�ҳ���Һ�����Ϊ400mL�����ҳ�����Һ��H+��Ũ��Ϊ???��
�ο��𰸣���9�֣���1��?��?��? 4 OH- - 4 e-? = O2 �� + 2H2O ��
4AgNO3+2H2O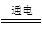 ?4Ag+ O2��+4HNO3�� CH4-8e-+10OH-= CO32-+7H2O ��
?4Ag+ O2��+4HNO3�� CH4-8e-+10OH-= CO32-+7H2O ��
��2��? 0.224 L��? 0.1mol/L?��ÿ��1�֣�
�����������1������ȼ�ϵ�أ�ͨ�����ĵ缫�Ǹ�����ͨ��������������������M��������N�����������ڹ���ʱM��N�����缫�������������٣�����M������N��ʯī����Һ��OH���ŵ磬������缫��Ӧʽ��4 OH- - 4 e- = O2 �� + 2H2O�����ҳ����ܵķ�Ӧʽ��4AgNO3+2H2O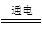 ?4Ag+ O2��+4HNO3������ԭ����е������Һ�Լ��ԣ����Ը����ĵ缫��Ӧʽ��CH4-8e-+10OH-= CO32-+7H2O ��
?4Ag+ O2��+4HNO3������ԭ����е������Һ�Լ��ԣ����Ը����ĵ缫��Ӧʽ��CH4-8e-+10OH-= CO32-+7H2O ��
��2��4.32g�������ʵ�����0.04mol����ת�Ƶ�����0.04mol�����Ը��ݵ��ӵĵ�ʧ�غ��֪������0.01mol��������״���µ�;����0.224L�������ҳ��е��ܷ�Ӧʽ��֪����ʱ����������0.04mol�����������ӵ�Ũ����0.04mol��0.4L��0.1mol/L��
�����Ѷȣ�һ��
2��ѡ���� �������⣩��ͼ��пƬ��ͭƬͬʱ����ϡ2.����������ɵ�ԭ���װ�ã�c��dΪ�����缫���������йص��ж���ȷ����?
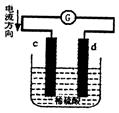
A��dΪ����������������Ӧ
B��cΪͭƬ��ͭƬ�Ϸ�����ԭ��Ӧ
C����ع����Ĺ����У�d�缫�ϲ�������������
D����ع����Ĺ����У���Һ��pH����
�ο��𰸣�CD
�������������ԭ��صĸ���й��жϡ���ԭ����нϻ��õĽ���������ʧȥ���ӣ�������������������Ӧ�������õĽ�����������������ʧȥ�ĵ��Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ����������ϵõ����ӣ�������ԭ��Ӧ�����Ը���װ��ͼ���ж�c�Ǹ�����d���������������������ϵõ����ӣ�������ԭ��Ӧ�������������Դ���CD��
�����Ѷȣ���
3��ѡ���� ��������ʵ���������ý�����ȷ����
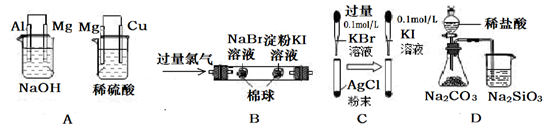
ʵ��
| ʵ������
| ����
|
A
| ����ձ���þ���������ݣ��ұ��ձ���ͭ����������
| ��ԭ�ԣ� Al��Mg��Cu
|
B
| �������Ϊ��ɫ���ұ�����Ϊ��ɫ
| �����ԣ�Cl2��Br2��I2
|
C
| �Թ��а�ɫ�����ȱ䵭��ɫ�����Ϊ��ɫ
| ����ת����ʵ�ʾ��dz����ܽ�ƽ����ƶ�
|
D
| ��ƿ��������������ձ�����Һ�����
| �ǽ����ԣ�Cl��C��Si
|
�ο��𰸣�C
���������A������ձ�����������NaOH��Һ��Ӧ��������������þ���������������ݣ��ұ��ձ��У�þ������ϡ���ᷴӦ��þ��������ͭ��������ͭ���������ݣ�ʵ��������ȷ�������۴��Ƚ�ʱ���õ��Լ���ͬ���ó��˴���Ľ��ۣ�A�����������Ϊ��ɫ����˵�������ԣ�Cl2��Br2�����ұ�����Ϊ��ɫ����ȷ��������KI�����˷�Ӧ���п�����Cl2��KI�����˷�Ӧ��B�������ɫ��������Һ���ټ������KBr��Һ���ٵ���KI����ɫ�����ȱ䵭��ɫ����ɫ��˵����������ת����һ����ƽ���ƶ��Ľ����C�ԣ�Ҫͨ���ȽϷǽ����γɵ��������ǿ�����ȽϷǽ����Ե�ǿ���Ļ���һ��Ҫ�Ƚ���ۺ����������ǿ���������Cl����ۺ����ᣬD����ѡC��
���㣺�����ԡ��ǽ����Ե�ǿ���ıȽ϶ϣ������ܽ�ƽ���Ӧ�á�
�����Ѷȣ�����
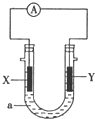
4��ѡ���� ��ͼ��XΪ���ʹ裬YΪ��������aΪNaOH��Һ����ͼ��װһ��ԭ��أ�����˵����ȷ���ǣ�������
A��XΪ�������缫��ӦΪ��Si-4e-�TSi4+
B��XΪ�������缫��ӦΪ��4H2O+4e-�T4OH-+2H2��
C��XΪ�������缫��ӦΪ��Si+6OH--4e-�TSiO32-+3H2O
D��YΪ�������缫��ӦΪ��Fe-2e-�TFe2+