|
高考化学必考知识点《物质的量》试题强化练习(2017年最新版)(六)
2017-08-06 11:24:42
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 &nb 91exam .orgsp;(1)下列物质中,物质的量最大的是________,含原子个数最多的是________,质量最大的是________。
A.3gH2;
B.标况下33.6LCO2;
C.1.204×1024个HCl分子;
D.49gH2SO4;E.46g乙醇(C2H5OH);F.4℃时10mL水
| (2)在一定条件下,32gA和22gB恰好反应生成C和9gD,在相同条件下,8gA和足量B反应生成D和0.125molC,从上述事实可推知C的摩尔质量为?。
参考答案:(1)C? E? C?(2)90g/mol
本题解析:(1)C选项的物质的量为2mol,物质的量最大。E选项原子的个数为9NA,原子个数最多。C的质量为73g ,质量最大。(2)因为32 gA和22 gB恰好反应生成C和9 gD,可以得到C的质量为32+22―9="45g" ,现有8gA反应生成C的质量为11.25g。代入M=m/n,则可以得到C的摩尔质量为90g/mol。
本题难度:一般
2、简答题 三大强酸的性质均与浓度有关.回答下列问题:
(1)某学习小组用15mol/L浓硝酸配制100mL 3mol/L稀硝酸.
①他们需要用量筒量取15mol/L浓硝酸______mL;
②如图所示仪器,在配制过程中不需用的是______(填序号).
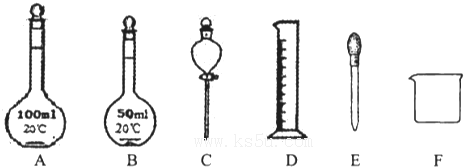
除图中已有的仪器外,配制上述溶液还需用到的玻璃仪器是______;
③下列实验操作中,不正确的是______(填写标号).
A.使用容量瓶前,检查它是否漏水.
B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出.
C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容.
D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀.
④用量筒量取浓硝酸,读数时,俯视量筒,所配制溶液的浓度______(填“偏高、偏低、无影响”).
(2)①铜与浓硫酸在加热条件下反应,浓硫酸表现出来的性质是______.
②MnO2与浓盐酸在加热条件下反应,离子方程式为______.
③分别用浓硝酸和稀硝酸制取相同质量Cu(NO3)2晶体,消耗浓硝酸和稀硝酸的物质的量之比是______.
参考答案:(1)①设需要浓硝酸的体积为V,则0.1L×3mol/L=15mol/L×V,V=0.02L=20.0mL,
故答案为:20.0mL;
②配制100mL 3mol/L稀硝酸需要量筒、烧杯、玻璃棒、胶头滴管以及容量瓶等仪器,则不需要的仪器为50mL容量瓶、分液漏斗,还缺少玻璃棒,
故答案为:BC;玻璃棒;
③A.容量瓶有瓶塞,配制过程中需要摇匀,所以使用容量瓶前,检查它是否漏水,故A正确;
B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出,导致配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,故B错误;
C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容;容量瓶只能用于配制一定浓度的溶液,不能用于稀释或者加热,故C错误;
D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀,该存在符合配制要求,故D正确;
故选BC;
④用量筒量取浓硝酸,读数时俯视量筒,导致量取的浓硝酸的体积偏小,配制的溶液中溶质的物质的量偏小,所配制溶液的浓度偏低,
故答案为:偏低;
(2)①铜与浓硫酸在加热条件下反应方程式为:Cu+2H2SO4(浓)△.CuSO4+SO2↑+2H2O,该反应中,浓硫酸将铜氧化成铜离子,浓硫酸表现了氧化性;反应产物中有硫酸铜和水生成,所以浓硫酸有表现了酸性,
故答案为:氧化性和酸性;
②二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,反应的离子方程式为MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-△.Mn2++Cl2↑+2H2O;
③设制取的硝酸铜的物质的量为nmol,根据反应的相关方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3(稀)=3Cu(NO3)2+2NO2↑+4H2O可知,需要浓硝酸的物质的量为:4nmol,需要稀硝酸的物质的量为:83nmol,则消耗浓硝酸和稀硝酸的物质的量之比是:4nmol:83nmol=3:2,
故答案为:3:2.
本题解析:
本题难度:一般
3、选择题 下列两种气体的分子数一定相等的是
A.质量相等、密度不同的N2和C2H4
B.体积相等的CO和N2
C.等温、等体积的O2和N2
D.等压、等体积的N2和CH4
参考答案:A
本题解析:N2和C2H4这两种气体的摩尔质量相等,质量相等时,物质的量也就相等,所含的分子数也一定相等,A项正确。B、C、D项可根据阿伏加德罗定律及其推论加以判断,所含分子数均不一定相等。答案选A。
本题难度:一般
4、计算题 使一定的磷化氢和氢气的混合气体,依次通过两支加热的硬质玻璃管,第一支玻璃管中装有铜屑,第二支玻璃管中装有氧化铜,第一支玻璃管中由于发生如下反应:2PH3+3Cu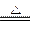 Cu3P2(s)+3H2,玻璃管质量增加4.96 g,第二支玻璃管中发生反应后质量减少了5.76 g。 Cu3P2(s)+3H2,玻璃管质量增加4.96 g,第二支玻璃管中发生反应后质量减少了5.76 g。
(1)计算原混合气体中,磷化氢和氢气的体积比。
(2)在标准状况下,原混合气体的密度是多少?
参考答案:(1)4∶3? (2)0.91 g・L-1
本题解析:设PH3、H2的物质的量分别为x mol、y mol。
2PH3+3Cu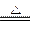 Cu3P2(s)+3H2?增重 Cu3P2(s)+3H2?增重
2 mol? 3 mol? 62 g
x mol?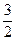 x mol? 31x g x mol? 31x g
31x g="4.69" g
x=0.16
H2+CuO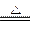 H2O+Cu?减少 H2O+Cu?减少
1 mol? 16 g
(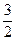 x+y) mol? 16( x+y) mol? 16(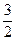 x+y) g x+y) g
16(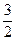 x+y) g="5.76" g x+y) g="5.76" g
y=0.12
(1)V(PH3)∶V(H2)="0.16" mol∶0.12 mol=4∶3
(2)标准状况下,混合气体的密度为
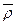 (混)= (混)=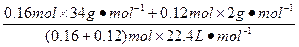 ="0.91" g・L-1。 ="0.91" g・L-1。
本题难度:简单
5、简答题 标准状况下,CO2和CO的混合气体7.2g,体积为4.48L,则此混合气体中CO2和CO的物质的量各是多少?
参考答案:标准状况下,混合气体的物质的量为:4.48L22.4L/mol=0.2mol,
设CO的物质的量为x,CO2的物质的量为y,则:
本题解析:
本题难度:一般
|