微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
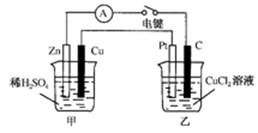
(1)甲装置的名称是_______;乙装置的名称是_______;Zn为_______极;Pt为______极。
(2)写出电极反应式:Cu极________________;C极________________。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色______(填“变深”、“变浅”或“无变化”)。
(4) 若乙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将________(填“增大”、“减小”或“不变”,下同);乙中溶液的pH将________。
参考答案:(1)甲装置名称是原电池;乙装置名称是电解池;Zn为负极;Pt为阳极。
(2) Cu极2H++2e-=H2↑;C极Cu2++2e-=Cu。
(3)乙中溶液的颜色无变化
(4)甲中溶液的pH将增大;乙中溶液的pH将增大
本题解析:(1)甲池为锌铜原电池,活性较强的锌做负极,铜为正极;与外电源正极相连的Pt电极为阳极,碳棒为阴极
(2)Cu极:2H++2e-=H2↑;?C极:Cu2++2e-=Cu
(3)乙池中电极都换成铜电极时,阳极:Cu―2e-=Cu2+;阴极:Cu2++2e-=Cu,即溶液中Cu2+的浓度不改变,溶液的颜色无变化
(4)甲池中总反应Zn+2H+=Zn2++H2↑,H+浓度减小,酸性减弱,pH增大;而乙池中总反应为:2Cl-+2H2O=H2↑+Cl2↑+2OH-,OH-离子浓度增大,碱性增强,pH增大
本题难度:一般
2、选择题 由化学能转变的热能或电能仍然是人类使用的主要能源.根据下图所示的装置,判断下列说法不正确的是
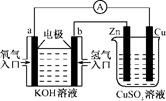
A.该装置中Cu极为阳极
B.当铜片的质量变化了12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L
C.该装置中b极的电极反应式是:H2+2OH--2e-===2H2O
D.该装置中a极为正极,发生氧化反应
参考答案:D
本题解析:根据装置可判断,左侧是原电池,右侧是电解池。a极通入氧气,所以a极是正极,则铜是阳极,A正确,D不正确;12.8g铜是0.2mol,转移电子是0.4mol。根据电子的得失守恒可知,氧气是0.1mol,B正确;b极通入氢气,作负极,失去电子,C正确,答案选D。
本题难度:一般
3、选择题 电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0-6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水作用。其原理如图所示。下列说法正确的是
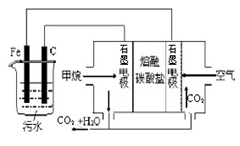
A.铁电极为阳极,反应式为:Fe-3e-= Fe3+
B.通入甲烷的石墨电极作负极,反应式为:CH4+8OH--8e-=CO2+6H2O
C.为增强污水的导电能力,可向污水中加入适量乙醇
D.若阴极产生了44.8L气体,则理论上消耗同条件下的甲烷为11.2L
参考答案:D
本题解析:A、铁电极为阳极,反应式为:Fe-2e-= Fe2+,错误;B、通入甲烷的石墨电极作负极,反应式为:
CH4+4CO32--8e-=5CO2+2H2O,错误;C、乙醇是非电解质,不能增强导电性,错误;D阴极产生氢气44.8L ,若在标况下是2mol,转移4摩尔电子,消耗0.5molCH4,标况下就是11.2L,正确。
本题难度:一般
4、选择题 下列有关金属铁的腐蚀与防护,说法正确的是( )
A.酸雨后易发生析氢腐蚀、炒锅存留盐液时易发生吸氧腐蚀
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.铁与电源正极连接可实现电化学保护
D.将钢管与铜管一起堆放时可保护钢管少受腐蚀
参考答案:A、酸雨后电解质环境是酸性较强的,易发生析氢腐蚀,炒锅存留盐液时的电解质为中性,金属易发生吸氧腐蚀,故A正确;
B、镀锡铁和镀锌铁镀层破损时,前者是金属铁为负极,后者是金属锌为负极,前者更易被腐蚀,故B错误;
C、铁与电源正极连接金属铁做阳极,易被腐蚀,故C错误;
D、将钢管与铜管一起堆放,形成原电池中,金属铁为负极,所以钢管易腐蚀,故D错误.
故选A.
本题解析:
本题难度:简单
5、选择题 下列叙述不正确的是( )
A.铁表面镀锌,铁作阳极
B.船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-=4OH-
D.工业上电解饱和食盐水的阳极反应:2Cl--2e-=Cl2
参考答案:A、铁表面镀锌,镀层是锌,应作阳极;镀件是铁,应作阴极,故A错误.
B、船底镶嵌锌块,锌、铁和海水构成原电池,锌作负极,铁作正极,锌被腐蚀从而保护了铁,故B正确.
C、钢铁的吸氧腐蚀中,正极上氧气得电子发生还原反应和水生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,故C正确.
D、工业上电解饱和食盐水时,氯离子的放电能力大于氢氧根离子,所以阳极上氯离子失电子生成氯气,电极反应式为:2Cl--2e-=Cl2↑,故D正确.
故选A.
本题解析:
本题难度:简单