��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� [��ѧһѡ��3:���ʽṹ������](15�֣�
һˮ�����İ���ͭ��II)(��ѧʽΪ ��һ����Ҫ��Ⱦ�ϼ�ũҩ�м��塣ijѧϰС���Կ�ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3,������Fe2O3��SO2���ʣ�Ϊԭ���Ʊ������ʵ��������£�
��һ����Ҫ��Ⱦ�ϼ�ũҩ�м��塣ijѧϰС���Կ�ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3,������Fe2O3��SO2���ʣ�Ϊԭ���Ʊ������ʵ��������£�
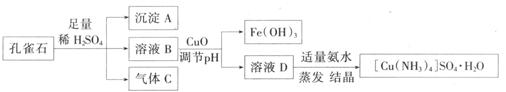
��ش�
(1) ����A�ľ�������С���ϵ�ԭ�Ӹ���Ϊ______������C������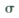 ����
����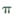 ���ĸ�����Ϊ______
���ĸ�����Ϊ______
(2) ��ҺD�����������ӵĿռ乹��Ϊ______��������ԭ�ӵ��ӻ��������Ϊ______
(3) MgO���۵����CuO��ԭ��Ϊ____________
(4) ����һˮ�����İ���ͭ��II)��������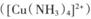 ����λ��____________��
�����____________��
(5)ʪ����ͭ����������ҺD�Ƶ�ͭ���ʣ�ͭ���ʾ�����ԭ�ӵĶѻ���ʽ��ͼ����ʾ���侧����ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ��ͼ����ʾ��
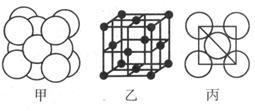
��ͭ���ʾ�����ԭ�ӵĶѻ���ʽΪ____________��������Cuԭ�ӵ���λ��Ϊ______
����Cuԭ�Ӱ뾶Ϊacm����Cu���ʾ�����ܶ�Ϊ______g/cm3(ֻ�г�����ʽ�������ӵ�������ֵΪNA)��
�ο��𰸣���1��12?��2�֣�? 1��1?��2�֣�?��2���������壨1�֣�? sp3 ��1�֣�?
(3)MgO�ľ����ܴ�2�֣�����������Ҳ�ɸ��֣���4��? ?��2�֣�
?��2�֣�
��5���������������ܶѻ���1�֣���12 ��1�֣���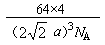 ��3�֣�����������Ҳ���֣�
��3�֣�����������Ҳ���֣�
�����������1����ȸʯ�еĶ�������������Ӧ�����Գ���A�Ƕ������衣����������ԭ�Ӿ��壬��������С���ϵ�ԭ�Ӹ���Ϊ12����C��CO2���壬�����к���̼��˫��������˫������1��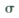 ����1��
����1��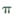 �����ɵģ����ɶ��ߵĸ���֮����1�U1�ġ�
�����ɵģ����ɶ��ߵĸ���֮����1�U1�ġ�
��2����Һ��D������ͭ����������SO42����������֪��ԭ�Ӻ��еŶԵ����ǣ�6��2��2��4����2��0����û�й¶Ե��ӣ���������������ṹ������sp3�ӻ���
��3������þ������ͭ�γɵľ��嶼�����Ӿ��壬þ���Ӱ뾶С��ͭ���ӵģ���������þ��MgO�ľ����ܴ��۵�ߡ�
��4��һˮ�����İ���ͭ�������ǰ�������߹¶Ե��ӣ�ͭ�ṩ�չ�������Խṹʽ�ǣ����𰸣���
��5����ͭ�������������ܶѻ������ݼ�ͼ��֪����ͭԭ�Ӿ��������ԭ�ӹ���3��8��2��12����������λ����12��
�ڸ�����ͼ��֪��һ��������ͭԭ�ӵ���ĿΪ8��1/8��6��1/2��4�����ݱ�ͼ��֪�������ı߳��� ��������
��������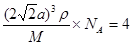 ����æѣ�
����æѣ�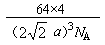 ��
��
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ�?��?
A. C ��N��O�ĵ�һ��������������?
B. NH3��H3O+��NH4+?���������
C. P4�� CCl4�� CH4 ��Ϊ��������ṹ�����Ǿ�Ϊ109��28��
D.HClO?�� HClO3?��?HClO4������������ǿ
�ο��𰸣�D
�����������̬�����Ի�̬ԭ��ʧȥ1������ת��Ϊ��̬��̬����������Ҫ���������������һ�����ܣ�ͬ����Ԫ���������ҵ�һ��������С��A����ȷ�������в�������λ����B����ȷ���������м�����60�㣬������ȷ�Ĵ���D��
�����Ѷȣ���
3������� ������(Na3N)�ǿ�ѧ���Ʊ���һ����Ҫ�Ļ��������ˮ���ÿɲ���NH3����ش��������⣺
(1)Na3N�ĵ���ʽ��_______���û�������_______���γɵġ�
(2)Na3N�����ᷴӦ����_____���Σ������ʽ��______��
(3)Na3N��ˮ�ķ�Ӧ����________��Ӧ��
(4)�Ƚ�Na3N���������ӵİ뾶��r(Na+)______r(N3-)������ڡ� �����ڡ���С�ڡ�����
�ο��𰸣�(1)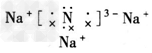 ������
������
(2)2��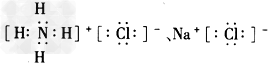
(3)���ֽ�
(4)��
���������
�����Ѷȣ�һ��
4��ѡ���� ���л�ѧʽ�ȱ�ʾ���ʵ�Ԫ����ɣ��ֱ�ʾ���ʵķ�����ɵ���
A��NH4NO3
B��SiO2
C��C6H5NO2
D��Cu
�ο��𰸣�C
���������ֻ�з��Ӿ���Ļ�ѧʽ�����ܼȱ�ʾ���ʵ�Ԫ����ɣ��ֱ�ʾ���ʵķ�����ɣ�����ѡ��C��ȷ��A�����Ӿ��壬B��ԭ�Ӿ��壬D�ǽ������壬��ѡC��
�����Ѷȣ�һ��
5������� ����������ȷ���ǣ�������
A�����ӻ������в����ܺ��й��ۼ�
B�����ۻ������в����ܺ������Ӽ�
C���Ǽ��Է�����һ�����зǼ��Լ�
D���ɼ��Լ��γɵķ���һ���Ǽ��Է���
�ο��𰸣�A�����ӻ������п��ܺ��й��ۼ�����NaOH�ȣ���A����
B�����ۻ�������һ���������Ӽ�����B��ȷ��
C���Ǽ��Է����п��ܲ����Ǽ��Լ�����CCl4�ȣ���C����
D���ɼ��Լ��γɵķ��ӿ����ǷǼ��Է��ӣ���CO2��CCl4�ȣ���D����
��ѡB��
���������
�����Ѷȣ�һ��