|
高中化学必备知识点《认识晶体》考点特训(2017年冲刺版)(八)
2017-08-06 11:48:33
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,
具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们
的晶体结构如图所示。
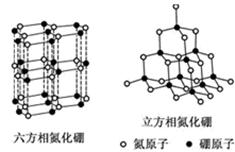
(1)关于这两种晶体的说法,正确的是?(填序号)。
A.立方相氮化硼含有σ键和π键,所以硬度大
B.六方相氮化硼层间作用力小,所以质地软
C.两种晶体中B-N键均为共价键
D.两种晶体均为分子晶体
| (2)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为?,其结构与石墨相似却不导电,原因是?。
(3)立方相氮化硼晶体,硼原子的杂化轨道类型为?。该晶体的天然矿物在青藏高原地下约300 km在古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是?。
(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 molNH4BF4含有 ?mol配位键。
参考答案:(1)B、C (2)平面三角形;层状结构中没有自由移动的电子;
(3)sp3;(4)高温、高压;(5)2
本题解析:(1)A.立方相氮化硼只含有σ键,由于形成的是立体网状结构,所以硬度大,错误;B.六方相氮化硼层间以分子间作用力结合,作用力小,所以质地软,正确;C.两种晶体中B-N键均为共价键,正确;D.两种晶体前者是混合晶体,后者是原子晶体,错误。(2)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为平面三角形;其结构与石墨相似却不导电,原因是层状结构中没有自由移动的电子;(3)立方相氮化硼晶体,硼原子的杂化轨道类型为sp3;根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是高温、高压条件;(4)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 molNH4BF4含有N与H原子间和B与F原子间形成的2个配位键。
本题难度:一般
2、选择题 某离子化合物的晶胞如图所示立体结构,晶胞是整个晶体中最基本的重复单位。阳离子位于此晶胞的中心,阴离子位于8个顶点,该离子化合物中,阴、阳离子个数比是?
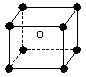
[? ]
A.?1∶8?
B.?1∶4? ?
C.?1∶2?
D.?1∶1
参考答案:D
本题解析:
本题难度:一般
3、选择题 仔细观察下图,它表示的是晶体还是非晶体

[? ]
A.是晶体
B.可能是晶体,可能是非晶体
C.是非晶体
D.不能确定
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列说法正确的是( )
A.冰融化时,分子中H―O键发生断裂
B.分子晶体中,分子间作用力越大,通常熔点越高
C.分子晶体中,共价键键能越大,分子的熔、沸点越高
D.分子晶体中,分子间作用力越大,分子越稳定
参考答案:B
本题解析:冰融化时,分子中H―O键没有发生断裂,分子间的作用力破坏了,分子晶体中,分子间作用力越大,通常熔点越高。同类型的分子晶体中,非金属性越强,分子越稳定。
本题难度:简单
5、填空题 下表为长式周期表的一部分,其中的编号代表对应的元素。
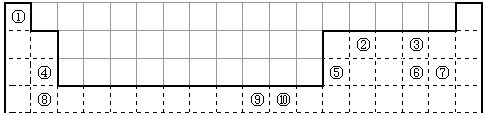
请回答下列问题
(1)表中属于d区的元素是________________(填编号)。
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为_________________(用对应的元素符号表示)。
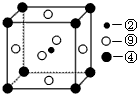
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是__________________。
A.分子中含有氢键
B.属于非极性分子
C.含有4个σ键和1个π键
D.该氢化物分子中,②原子采用sp2杂化
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_________;该元素与元素①形成的分子X构形为______________;X在①与③形成的分子Y中的溶解度很大,其主要原因是__________________________。
(5)A、B均为短周期金属元素。依据下表数据,写出B原子的电子排布式:__________________
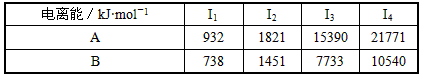
(6)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或
d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+
_____________颜色(填“无”或“有”)。
参考答案:(1)⑨
(2)MgCNi3或CMgNi3
(3)BD
(4)1;三角锥形;X和Y都是极性分子(且能形成氢键),根据相似相溶原理,极性分子易溶于极性溶剂中
(5)1s22s22p63s2
(6)有
本题解析:
本题难度:困难
|