微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某研究性学习小组研究HNO3的氧化性,设计了如下实验:在盛有新配制FeS04溶液的试管中滴入2滴KSCN溶液,观察现象,然后再滴人几滴浓HN 03,溶液的颜色变红,但是将红色溶液放置一会儿则发现溶液由红色突然变为蓝色,并产生红棕色气体。这一奇 特现象激起了同学的好奇心与求知欲望,对此现象设计了探究性实验。
(1)实验室粗略配制一定质量分数的硫酸亚铁溶液的方法是:将一定质量的绿矾(FeS04・7H2 0)置于烧杯中,__________________________。
(2)提出假设:
甲同学认为是FeS04与HN03作用
乙同学认为是KSCN与HNO3作用
(3)根据乙同学的观点,设计了如下实验方案进行验证:向浓HN03中逐滴加入KSCN溶液,实验开始时无明显现象,一段时间后溶液慢慢变红色至深红色,突然剧烈反应产生大量气泡,放出红棕色气体。继续滴入KSCN,溶液变为浅蓝色,最后变成无色。将产生的气体通人过量的Ba(OH)2溶液,产生浑浊,并剩余一种气体(该气体是空气中的主要成分之一);向反应后的溶液中加入BaC12溶液产生白色沉淀。
写出向浓HNO3中滴入KSCN溶液反应的离子方程式:__________________
丙同学认为还应设计K2S04溶液与浓硝酸作用的实验,他的理由是__________________
(4)延伸探究:丁同学认为SCN-的性质还应进一步探究,查资料发现:(SCN)2是一种“拟卤素”,与C12、Br2有相似的性质。他据此设计了以下方案:向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均变为黄色。请写出Fe(SCN)3与氯气反应的离子方程式:?。
(5)通过本次探究,可以得出以下结论:
a、用SCN -间接检验Fe2+时加入氧化剂应注意?(填“少量”、“过量”);
b、与SCN-反应使溶液变红的不一定是Fe3+
参考答案:(1)加入适量的稀硫酸,用玻璃棒搅拌,(再加水稀释,)最后加入少量铁粉(或铁屑)
(3)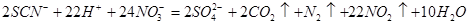
对照实验(验证硫酸钾与浓硝酸是否反应)。
(4)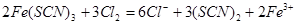
(5)少量
本题解析:(1)实验室粗略配制一定质量分数的硫酸亚铁溶液的方法是:将一定质量的绿矾(FeS04・7H2 0)置于烧杯中,加入适量的稀硫酸,用玻璃棒搅拌,(再加水稀释,)最后加入少量铁粉(或铁屑,这是为了防止亚铁离子被氧化);(3)突然剧烈反应产生大量气泡,放出红棕色气体,该气体为二氧化氮,通入过量的Ba(OH)2溶液,产生浑浊,并剩余一种气体(该气体是空气中的主要成分之一),说明了含有硫酸根离子,该气体为氮气,并且可以判断出碳元素被转化为二氧化碳,所以向浓HNO3中滴入KSCN溶液反应的离子方程式为 ;设计K2S04溶液与浓硝酸作用的实验作为对照实验(验证硫酸钾与浓硝酸是否反应);(4)向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均变为黄色,说明生成了(SCN)2,所以与氯气反应的离子方程式为:
;设计K2S04溶液与浓硝酸作用的实验作为对照实验(验证硫酸钾与浓硝酸是否反应);(4)向Fe(SCN)3中分别滴加过量的氯水、溴水,溶液的红色均变为黄色,说明生成了(SCN)2,所以与氯气反应的离子方程式为: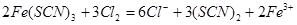 ,所以用SCN -间接检验Fe2+时加入氧化剂应注意少量,与SCN-反应使溶液变红的不一定是Fe3+。
,所以用SCN -间接检验Fe2+时加入氧化剂应注意少量,与SCN-反应使溶液变红的不一定是Fe3+。
点评:本题以铁离子的检验的实验为模型,结合实验过程中出现的试剂问题,设计了一个探究性的实验,本题有利于培养学生的探究性思维,本题综合性好,有一定的难度。
本题难度:一般
2、选择题 有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。⑴将该粉末溶于水得无色溶液和白色沉淀;⑵在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;⑶取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰。由上述现象可推断:
A.可能有Na2CO3
B.一定有Na2SO4
C.一定无NaCl
D.一定有K2SO4
参考答案:B
本题解析:溶于水得无色溶液和白色沉淀,说明一定没有氯化铜,一定含有硝酸钡。滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体,说明含有碳酸钡和硫酸钡沉淀。根据焰色反应可知,含有钠离子,没有钾离子,及一定含有碳酸钠和硫酸钠,没有硫酸钾和碳酸钾,而氯化钠不能确定,答案选B。
本题难度:一般
3、选择题 鉴别某种白色织物是否是蚕丝制品,可选用的适宜方法是(? )
A.滴加盐酸
B.滴加浓硫酸
C.滴加氢氧化钠溶液
D.滴加浓硝酸
参考答案:D
本题解析:蛋白质遇到浓硝酸会发生显色反应,显示黄色,据此可以鉴别某种白色织物是否是蚕丝制品,答案选D。
点评:该题贴近生活,基础性强,有利于调动学生的学习兴趣。该题的关键是熟练记住蛋白质的性质,然后灵活运用即可。
本题难度:简单
4、选择题 下列叙述正确的是
A.标准状况下,1 mol任何物质的体积约为22.4 L
B.1 mol气体的体积约为22.4 L
C.1 molNe和1 molO2体积相同
D.标准状况下,1 molNe和Cl2的混合气体(任意体积比)的体积约为22.4 L
参考答案:D
本题解析:对于气体摩尔体积的定义,应注意两个问题:一是仅指气体体积,而非液体或固体的体积;二是在标准状况下,气体的摩尔体积的具体值为22.4 L・mol-1,而在不同温度和压强下,气体摩尔体积并不相同.
本题难度:一般
5、选择题 要将溴水中的溴提取出来,需要用到的一组仪器是
[? ]
A.普通漏斗、玻璃棒、烧杯
B.分液漏斗、玻璃棒、烧杯
C.大试管、试管夹、容量瓶
D.分液漏斗、烧杯、铁架台
参考答案:D
本题解析:
本题难度:简单