微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于如图所示装置的叙述,正确的是
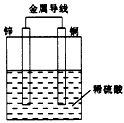
[? ]
A.铜是阳极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面被还原
参考答案:D
本题解析:
本题难度:一般
2、选择题 X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
[? ]
A.X>Z>Y>M
B.X>Y>Z>M
C.M>Z>X>Y
D.X>Z>M>Y
参考答案:A
本题解析:
本题难度:一般
3、选择题 查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH―2e―→X+2H+.下列说法中正确的是( )
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2+4e―+2H2O=4OH―
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH + O2→2CH3CHO + 2H2O
参考答案:D
本题解析:A.根据同种电荷相互排斥,异种电荷相互吸引的原则,在电池内部H+由负电荷较多的正极移动。正确。B.通入氧气的电极为正极。在酸性条件下在正极发生的电极反应式为:O2+4e―+4H+ = 2H2O.错误。C.乙醇在负极发生反应,电子经过外电路流向正极。错误。D.根据题意及负极的电极式可知该电池总反应为:2CH3CH2OH + O2→2CH3CHO + 2H2O。正确。
本题难度:一般
4、选择题 锌―空气电池可能成为未来的理想动力源,该电池的电解质溶液可以是酸性或碱性。在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2 +2H2O。下列有关锌-空气电池说法正确的是
A.碱性电解质溶液中正极反应式为:4OH-- 4e-= O2↑+2H2O
B.碱性或酸性电解质溶液中,该电池正极反应式相同
C.该电池工作时,Na+移向负极
D.每生成1 mol ZnO22-转移电子数为2NA
参考答案:D
本题解析:A、碱性电解质溶液中正极应为O2得电子,错误;B、酸性溶液中正极反应式为:O2+4H++4e?=2H2O,碱性溶液中正极反应式为:O2+H2O+4e?=4OH?,正极反应式不同,错误;C、该电池工作时,Na+移向正极,错误;D、Zn元素化合价由0价升高至+2价,所以每生成1 mol ZnO22-转移电子数为2NA,正确。
本题难度:一般
5、选择题 用气体传感器可以检测汽车尾气中CO的含量。传感器是以燃料电池为工作原理,其装置如右图所示,该电池中电解质为氧化钇―氧化钠,其中O2-可以在固体介质NASICON中自由移动。下列说法错误的是

A.负极的电极反应式为:CO+O2- 2e-=CO2
2e-=CO2
B.工作时电子由电极a通过传感器流向电极b
C.工作时电极b作正极,O2-由电极a流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
参考答案:C
本题解析:原电池中负极失去电子,正极得到电子,所以CO在负极通入,空气在正极通入,即a是负极,b是正极。由于电解质为非水体系下的氧化钇―氧化钠,O2-可以在固体介质NASICON中自由移动,由正极流向负极。则:
A、负极的电极反应式为CO+O2--2e-=CO2,A正确;
B、工作时电子由负极a通过传感器流向正极b,B正确;
C、工作时电极b作正极,O2-由电极b流向电极a,C不正确;
D、传感器中通过的电流越大,说明参加反应的CO越多,因此尾气中CO的含量越高,D正确,答案选C。
本题难度:一般