微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 将m g固体NaHCO3加热分解一段时间后,质量变为n g。试求:
(1)尚未分解的NaHCO3的质量;
(2)生成的Na2CO3的质量;
(3)NaHCO3完全分解时的n值。
2、填空题 现有NaCl、Na2SO4、NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀和固体,从而实现阴离子的分离。相应的实验过程可用下图所示:
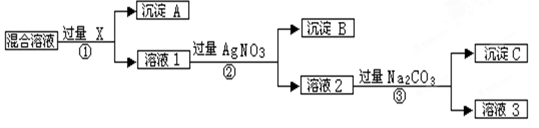
请回答下列问题:
⑴写出实验流程中下列物质的化学式:试剂X :?,沉淀A:?,沉淀B:??。
⑵上述实验流程中加入过量的Na2CO3的目的是?。
⑶按此实验方案得到的溶液3中肯定含有?(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的?,之后若要获得固体NaNO 3需进行的实验操作是?(填操作名称)。
3需进行的实验操作是?(填操作名称)。
3、选择题 下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量NaOH溶液和明矾溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
A.只有①④
B.只有③
C.只有②③
D.只有①③④
4、选择题 将4.34gNa、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到672mL混合气体,该混合气体通过放电,恰好完全反应,则它们的物质的量之比为
A.1:1:1
B.1:1:2
C.1:2:1
D.4:3:2
5、实验题 (10分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、N H4C1等物质
H4C1等物质 溶解度的差异,以食
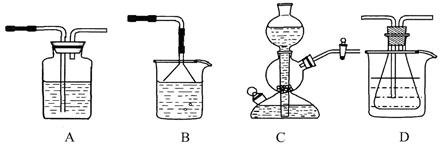
溶解度的差异,以食 盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、C、D四个装置可组装成实验室模拟 “侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳
盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、C、D四个装置可组装成实验室模拟 “侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳 酸钙;D:含氨的饱和食盐水、水
酸钙;D:含氨的饱和食盐水、水
四种盐在不同温度下的溶解度(g/100g水)表
?
| 0℃
| 10℃
| 20℃
| 30℃
| 40℃
| 50℃
| 60℃
| 100℃
|
NaCl
| 35.7
| 35.8
| 36.0
| 36_3
| 36.6
| 37.0
| 37.3
| 39.8
|
NH4HCO3
| 11.9
| 15.8
| 21.0
| 27.0
| ―①
| ―
| ―
| ―
|
NaHCO3
| 6.9
| 8.1
| 9.6
| 11.1
| 12.7
| 14.5
| 16.4
| ?
|
NH4Cl
| 29.4
| 33.3
| 37.2[ 来源:Z|xx| 来源:Z|xx|
| 41.4
| 45.8
| 50.4
| 55.3
| 77.3
|
(说明:①>35℃NH4HCO3会有分解)
请回答以下问题:
(1)装置的连接顺序应是?(填字母)。
(2)A装置中盛放的试剂是?,其作用是?。
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是?。
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去?杂质(以化学式表示)
( 5)将锥形瓶中的产物过滤后,所得的母液中含有?(以化学式表示),加入氯化氢,并进行?操作,使NaCl溶液循环使用,同时可回收NH4C1。
5)将锥形瓶中的产物过滤后,所得的母液中含有?(以化学式表示),加入氯化氢,并进行?操作,使NaCl溶液循环使用,同时可回收NH4C1。